
【题目】硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
[查阅资料] ①BCl3的熔点为-107.3 ℃,沸点为12.5 ℃;②2B+6HCl![]() 2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
[设计实验] 某同学设计如图所示装置制备三氯化硼:
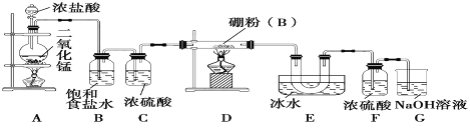
请回答下列问题:
(1)常温下,可用高锰酸钾与浓盐酸发生的反应可替代A装置中的反应,请写出高锰酸钾与浓盐酸反应的离子方程式:_______________________________________________。
(2)E装置的作用是________________________________。如果拆去B装置,可能的后果是______________________________________________________________________。
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式______________________________________________________。实验室保存三氯化硼的注意事项是___________________________________。
(4)实验中可以用一个盛装____________________(填试剂名称)的干燥管代替F和G装置,使实验更简便。
(5)为了顺利完成实验,正确的操作是_____(填序号)。
①先点燃A处酒精灯,后点燃D处酒精灯 ②同时点燃A、D处酒精灯 ③先点燃D处酒精灯,后点燃A处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓________________(填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
【答案】2MnO4-+10Cl-+16H+= 2Mn2++8H2O+5Cl2↑ 冷却和收集三氯化硼 硼粉与HCl反应生成的氢气与氯气混合,加热时易发生爆炸 BCl3+3H2O=H3BO3+3HCl↑ 隔绝空气,密封保存 碱石灰 ① NaOH
【解析】
(1)在A装置中用高锰酸钾固体粉末与浓盐酸发生反应可以制取氯气;
(2)在 E装置的作用是冷却和收集三氯化硼;如果拆去B装置,可能会发生反应2B+6HCl![]() 2BCl3↑+3H2↑,在D中加热氢气与氯气的混合气体,易发生爆炸;
2BCl3↑+3H2↑,在D中加热氢气与氯气的混合气体,易发生爆炸;
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,该反应的化学方程式是BCl3+3H2O=H3BO3+3HCl↑;因此在实验室保存三氯化硼的注意事项要隔绝空气,密封保存,防止受潮水解;
(4)F中浓硫酸防水蒸气进入E中使BCl3水解,G装置盛装氢氧化钠溶液吸收尾气,故实验中可以用一个盛装碱石灰的干燥管来代替F+G装置;
(5)①先点燃A处酒精灯,待整套装置中都充满Cl2后再点燃D处酒精灯,使之发生反应;
②若先点燃D处酒精灯,这时B就与装置中的空气发生反应得到B2O3,产生的BCl3产率和纯度降低;
③同时点燃A、D处酒精灯也会导致产生B2O3,影响制备BCl3;
(6)由于B的性质与Al相似,既能与强酸反应,也能与强碱反应放出氢气,所以取少量样品于试管中,滴加浓NaOH溶液,若有气泡产生,则样品中含有硼粉。
(1)在A装置中用高锰酸钾固体粉末与浓盐酸发生反应可以制取氯气,反应的离子方程式为:2MnO4-+10Cl-+16H+ = 2Mn2++8H2O+5Cl2↑;
(2)由于浓盐酸有挥发性,所以在氯气中含有HCl气体,用饱和NaCl溶液除去HCl杂质,用浓硫酸进行干燥,在D中发生反应:3Cl2+2B![]() 2BCl3;E装置的作用是冷却和收集三氯化硼;如果拆去B装置,可能会发生反应2B+6HCl
2BCl3;E装置的作用是冷却和收集三氯化硼;如果拆去B装置,可能会发生反应2B+6HCl![]() 2BCl3↑+3H2↑,在D中加热氢气与氯气的混合气体,易发生爆炸;
2BCl3↑+3H2↑,在D中加热氢气与氯气的混合气体,易发生爆炸;
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,该反应的化学方程式是BCl3+3H2O=H3BO3+3HCl↑;因此在实验室保存三氯化硼的注意事项要隔绝空气,密封保存,防止受潮水解;
(4)为防止BCl3水解在E与G之间连接一个盛有浓硫酸的装置;G装置中NaOH溶液吸收多余的Cl2,防止污染大气;在实验中也可以用一个盛装碱石灰的干燥管代替F和G装置,碱石灰既能吸收H2O(g)又能吸收Cl2,使实验更简便;
(5)①先点燃A处酒精灯,待整套装置中都充满Cl2后再点燃D处酒精灯,使之发生反应,正确;②若先点燃D处酒精灯,这时B就与装置中的空气发生反应得到B2O3,再点燃A处酒精灯产生的BCl3产率和纯度降低,错误;③同时点燃A、D处酒精灯也会导致产生B2O3,影响制备BCl3;答案选①。
(6)由于B的性质与Al相似,既能与强酸反应,也能与强碱反应放出氢气,所以取少量样品于试管中,滴加浓NaOH溶液,若有气泡产生,则样品中含有硼粉。


科目:高中化学 来源: 题型:
【题目】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:
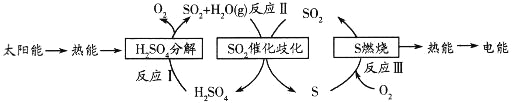
请回答下列问题:
(1)反应I的化学方程式为_____________________________________。1mol H2SO4(液)分解成气态物质需要吸收的能量是275.5kJ,硫的燃烧热为297 kJ·mol-1,则反应Ⅱ的热化学方程式为________________________________。
(2)单质硫也可以生成多硫化物实现能量间的转化。
①钠硫电池是一种新型高能电池,总反应为2Na+xS ![]() Na2Sx,该电池工作时的正极反应式为____________________,给该电池充电时,钠电极应与外电源的____________(填“正”或“负”)极相连接。
Na2Sx,该电池工作时的正极反应式为____________________,给该电池充电时,钠电极应与外电源的____________(填“正”或“负”)极相连接。
②多硫化合物H2S2O8中S的化合价为+6,分子中过氧键的数目为______________________。
③在碱性溶液中,多硫离子Sx2-被BrO![]() 氧化成SO
氧化成SO![]() ,
,![]() 被还原成Br-。该反应的离子方程式是________________________。
被还原成Br-。该反应的离子方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学方程式或离子方程式表示相应的化学反应.
(1)工业生产上将氯气通入石灰乳,在一定条件下蒸干可制漂白粉.写出该过程的化学方程式:___________________________________.
(2)侯氏制碱法中最后利用小苏打固体可以制得纯碱,写出该过程的化学方程式:____.
(3)向水玻璃溶液(Na2SiO3溶液)中,加入稀盐酸可用于生产硅酸胶体.用离子方程式表示该生产原理:________________________________________.
(4)硫酸工业中用氨水吸收二氧化硫,写出氨水吸收过量二氧化硫的离子方程式____.
(5)NO是大气污染物之一,目前一种治理方法是在400℃左右、在催化剂的作用下用氨气还原,写出化学方程式________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、乙酸,D中放有饱和碳酸钠溶液。
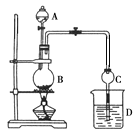
已知:①无水氯化钙可与乙醇形成微溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用为__________,圆底烧瓶中发生的化学反应方程式:_________。
(2)球形干燥管C的作用是_________,反应结束后D中的现象是_______________。
(3)该小组同学在实验时加入过量的乙醇,目的是_________________。
(4)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出____________;再加入(此空从下列选项中选择)________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是资源的宝库:合理利用海水资源是当今是世界研究的重点课题。结合所学知识回答下列问题:
(1)列举一项海水中的能源:__________ ,海水中储量最大的资源是________ ,获得该资源最古老的方法是____________。
(2)海水中还有大量NaCl,MgCl2等盐类物质,从海水中获得纯净NaCl的分离提纯方法有过滤、______。
(3)目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:
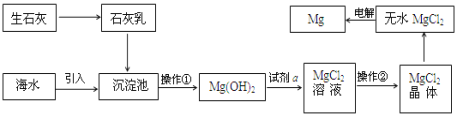
提示: MgCl2晶体的化学式为MgCl26H2O; MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
①操作②的名称___________、冷却结晶、过滤。
②用氯化镁电解生产金属镁的化学方程式为:_____________________。
(4)粗盐提纯后的的卤水中含有大量的溴,从中提取溴的部分过程如下:
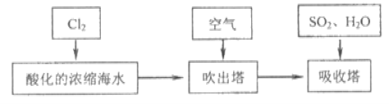
实验室模拟上述过程设计以下装置进行实验(所有橡胶制品已被保护,夹持装置已略去)
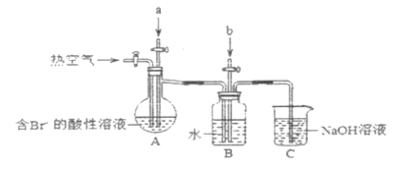
①A装置中通入a气体的目的是(用离子方程式表示) __________________________________________;
②A装置中先通入a气体后改通热空气。通入热空气的目的是______________________________________;
③B装置中b气体是SO2,目的是吸收富集Br2,此处离子方程式为___________________________________;
④向B装置中再次通入Cl2得到单质溴,对液体进行蒸馏,收集液溴。蒸馏应该选择下列仪器_____(填序号) 。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的镁和铜组成的混合物加入到过量的稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g。则下列叙述中错误的是
A. 当生成的沉淀量达到最大时,消耗NaOH溶液的体积V=100ml
B. 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
C. 参加反应的金属的总质量为9.6g>m>3.6g
D. 当金属全部溶解时收集到NO气体的体积在标准状况下一定为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于组成生物体的化学元素,下列叙述不正确的是
A. 组成生物体的化学元素,可以分成大量元素和微量元素
B. 组成不同生物体的化学元素不仅种类大体相同含量也基本相同
C. 组成生物体的化学元素,没有一种是生物界所特有的
D. 组成玉米和家兔的最基本元素都是碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验是化学学习的重要内容。根据你掌握的知识,完成下面内容。
![]() 实验室需要配制0.1 mol·L-1NaOH溶液230mL,请回答下列问题:
实验室需要配制0.1 mol·L-1NaOH溶液230mL,请回答下列问题:
![]() 应选择____mL的容量瓶,用天平称取____g NaOH。
应选择____mL的容量瓶,用天平称取____g NaOH。
![]() 溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中。若趁热转移会使溶液的浓度______(填“偏大”或“偏小”,下同);在洗涤烧杯和玻璃棒的过程中,每次洗涤液均需注入容量瓶,不能损失点滴液体,否则会导致溶液的浓度______。
溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中。若趁热转移会使溶液的浓度______(填“偏大”或“偏小”,下同);在洗涤烧杯和玻璃棒的过程中,每次洗涤液均需注入容量瓶,不能损失点滴液体,否则会导致溶液的浓度______。
![]() 有人认为,用这种方法只能配置0.1 mol·L-1的NaOH溶液,而无法得到0.1000 mol·L-1的NaOH溶液,你觉得他的理由是__________________________________________。
有人认为,用这种方法只能配置0.1 mol·L-1的NaOH溶液,而无法得到0.1000 mol·L-1的NaOH溶液,你觉得他的理由是__________________________________________。
![]() 选择下列实验方法分离物质,将分离方法的序号填在横线上。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
![]() 萃取分液
萃取分液 ![]() 升华
升华 ![]() 结晶
结晶 ![]() 过滤
过滤 ![]() 蒸馏
蒸馏 ![]() 分液
分液
![]() 分离饱和食盐水与沙子的混合物______;
分离饱和食盐水与沙子的混合物______;
![]() 从硝酸钾和氯化钠的混合液中获得硝酸钾______;
从硝酸钾和氯化钠的混合液中获得硝酸钾______;
![]() 从碘水中提取碘单质______;
从碘水中提取碘单质______;
![]() 分离水和汽油的混合物______;
分离水和汽油的混合物______;
![]() 分离
分离![]() 沸点为
沸点为![]() 和甲苯
和甲苯![]() 沸点为
沸点为![]() 的混合物______。
的混合物______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com