
(10分)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
Cu+2H2SO4(浓) CuSO4+A↑+2H2O
CuSO4+A↑+2H2O
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。则A应该属于______________(用字母代号填写)
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
A物质可以使酸性KMnO4溶液褪色,此反应中__________(填写化学式,下同) 失去电子,氧化剂
是____________。
(2)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的A气体在标准状况下体积为_________L (假设气体全部逸出)。
(3)将反应后所得到的溶液与足量Ba(OH)2溶液充分反应。请写出此过程发生的反应的离子方程式:______________________________________________________
计算反应后所得沉淀的质量为__________________g(保留到0.1g)。
(10分)(1)d;SO2;KMnO4(2) 2.24
(3)Ba2++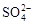 +2OH-+2H+=2H2O+BaSO4↓
+2OH-+2H+=2H2O+BaSO4↓
Ba2++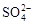 +2OH-+Cu2+=Cu(OH)2↓+BaSO4↓ 405.9
+2OH-+Cu2+=Cu(OH)2↓+BaSO4↓ 405.9
解析试题分析:(1) A物质可以导致酸雨的形成,所以根据元素的组成可知,A应该是SO2,SO2是酸性氧化物,答案选d。酸性高锰酸钾溶液具有强氧化性,能氧化SO2,作氧化剂,所以在反应中SO2失去电子,作还原剂。
(2)根据方程式可知,在反应中S元素的化合价从+6价降低到+4价,得到2个电子,所以如果该反应过程中转移了0.2mol电子,则生成0.1molSO2,在标准状况下的体积是2.24L。
(3)由于随着反应的进行,硫酸的浓度降低,而稀硫酸与铜是不反应。所以反应后的溶液中含有稀硫酸和硫酸铜,因此和氢氧化钡反应的方程式是Ba2++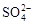 +2OH-+2H+=2H2O+BaSO4↓和Ba2++
+2OH-+2H+=2H2O+BaSO4↓和Ba2++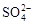 +2OH-+Cu2+=Cu(OH)2↓+BaSO4↓。原浓硫酸的物质的量是1.8mol,生成SO2是0.1mol,所以根据原子守恒可知,生成硫酸钡的物质的量是1.7mol,质量是1.7mol×233g/mol=396.1g。另外还生成0.1mol氢氧化铜,质量是0.1mol×98g/mol=9.8g,所以最终的沉淀质量是405.9g。
+2OH-+Cu2+=Cu(OH)2↓+BaSO4↓。原浓硫酸的物质的量是1.8mol,生成SO2是0.1mol,所以根据原子守恒可知,生成硫酸钡的物质的量是1.7mol,质量是1.7mol×233g/mol=396.1g。另外还生成0.1mol氢氧化铜,质量是0.1mol×98g/mol=9.8g,所以最终的沉淀质量是405.9g。
考点:考查根据方程式进行的有关计算
点评:在进行有关计算时,应该充分利用守恒法,例如电子得失守恒、原子守恒、电荷守恒、质量守恒等。


科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
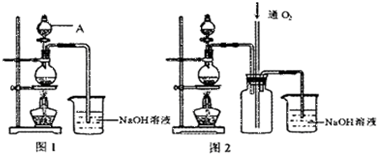
| 实验步骤 | 问题 |
| 1从U型管左端加入稀硝酸直至充满U型管右端 | ∥/ |
| 2用附有铜丝的胶塞塞住U型管右端,观察现象 | 现象是 有无色气体产生,右边溶液逐渐变成绿色 有无色气体产生,右边溶液逐渐变成绿色 |
| 3待反应停止后打开胶塞,观察实验现象 | 现象是 无色气体与空气接触后立即变成红棕色 无色气体与空气接触后立即变成红棕色 |
| 10-3a﹒V +0.5 |
| 0.14 |
| 10-3a﹒V +0.5 |
| 0.14 |
| 1 |
| 2 |
|
|
| 1 |
| 2 |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
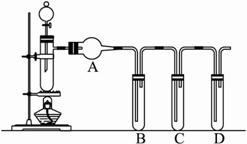
(1)装置气密性的检验须在盛放药品前进行。在上述装置中,往试管B、C、D中各加入5 mL蒸馏水封住导管口,各连接处都紧密而不漏气的情况下,点燃酒精灯,微热带支管的试管一会儿,试管B、C、D中未出现气泡;熄灭酒精灯后,试管B、C、D中导管内水面也未上升,其原因是: 。?
(2)①一般来说,硫酸的质量分数大于60%,就具有一定的氧化性,且越浓氧化性越强;②温度也要影响氧化性,如铜放于冷的浓硫酸中反应不明显,加热就可观察到明显现象。?
甲同学利用上述装置,用实验来验证硫酸氧化性的上述结论(已知98%的浓硫酸的密度为
1.84 g·cm -3)。他先向试管B加入5 mL品红试液,向试管C、D中各加入5 mL饱和澄清石灰水;向带支管的试管中放入铜粉和3 mL水,然后从分液漏斗向支管试管中滴加98%的浓硫酸10滴(约0.5 mL),加热至沸腾,这时支管试管中溶液颜色是否有明显变化 (填“无”或“有”),试用数据解释其原因 ;该同学用分液漏斗再向支管试管中加98%的浓硫酸10 mL,并加热至沸腾,观察到的现象分别是:支管试管中 ,B试管中 。?
(3)乙同学利用上述装置来检验浓硫酸和木炭粉在加热条件下发生反应的全部产物。?
①浓硫酸和木炭粉在加热条件下发生反应的化学方程式为: 。?
②要达此目的,则:?
A中加入试剂的名称是,作用是 ;?
B中加入试剂的名称是,作用是 ;?
C中加入试剂的名称是,作用是 ;?
D中加入试剂的名称是,作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
根据下图回答问题:
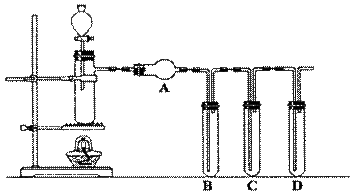
⑴装置气密性的检验须在盛放药品前进行。在上述装置中,往试管B、C、D中各加入5mL蒸馏水封住导管口,各连接处都紧密而不漏气的情况下,点燃酒精灯,微热带支管的试管一会儿,试管B、C、D中未出现气泡;熄灭酒精灯后,试管B、C、D中导管内水面也未上升,其原因是:____。
⑵①一般来说,硫酸的质量分数大于60%,就具有一定的氧化性,且越浓氧化性越强;②温度也要影响氧化性,如铜放于冷的浓硫酸中反应不明显,加热就可观察到明显现象。
甲同学利用上述装置,用实验来验证硫酸氧化性的上述结论(已知98%的浓硫酸的密度为1.84g?cm-3)。他先向试管B加入5mL品红试液,向试管C、D中各加入5mL饱和澄清石灰水;向带支管的试管中放入铜粉和3mL水,然后从分液漏斗向支管试管中滴加98%的浓硫酸10滴(约0.5mL),加热至沸腾,这时支管试管中溶液颜色是否有明显变化_____(填“无”或“有”),试用数据解释其原因____________;该同学用分液漏斗再向支管试管中加98%的浓硫酸10mL,并加热至沸腾,观察到支管试管中现象是____ _。
⑶乙同学利用上述装置来检验浓硫酸和木炭粉在加热条件下发生反应的全部产物。
①浓硫酸和木炭粉在加热条件下发生反应的化学方程式为:__________。
②要达此目的,则:
C中加入试剂的名称是_________,现象是_______________;
⑷利用上述装置探究锌与浓硫酸反应产物中有SO2和H2,D中加入试剂(名称): ;检验氢气方法 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com