
NO和CO都是汽车尾气里的有害物质,它们能缓慢地起反应生成氮气和二氧化2NO+2CO = N2+2CO2对此反应,下列叙述正确的是
A.冬天气温低,反应速率降低,对环境污染会更大
B.改变压强对反应速率没有影响
C.使用催化剂能促使反应正向进行
D.无论外界条件怎样改变,均对此化学反应的速率无影响
科目:高中化学 来源: 题型:
下列说法正确的是( )。
A.分子间作用力与化学键的键能大小相当
B.分子间作用力远强于化学键,是一种很强的作用
C.氢键主要影响物质的化学性质
D.分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间存在的相互作用称为分子间作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2 (g) + Cl2 (g) =2HCl (g) △H= ―184.6 kJ·mol-1,
则反应HCl (g)= 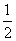 H2 (g) +
H2 (g) + 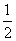 Cl2 (g) 的 △H 是
Cl2 (g) 的 △H 是
A.+184.6kJ/mol B.―92.3 kJ/mol
C.―369.2 kJ/mol D. +92.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下的可逆反应:2SO2(g)+O2(g)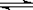 2SO3(g),若改变下列条件:①升高温度
2SO3(g),若改变下列条件:①升高温度
②增大压强 ③增大反应物浓度 ④加入催化剂,可提高反应物中的活化分子百分数的是
A.① ④ B.① ③ C. ② ③ D.①
查看答案和解析>>
科目:高中化学 来源: 题型:
向某一容积为5 L的密闭容器中,加入 0.2 mol CO和0.2 mol H2O,在800℃和催化剂存在的条件下,发生如下反应:CO(g)+H2O(g) 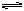 CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化关系如下图所示:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化关系如下图所示:
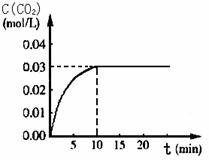
(1)由图中数据可知,反应从开始至达到平衡时,CO的化学反应速率v(CO)= ; H2的物质的量浓度c(H2)=_____________;该温度下此反应的平衡常数K = 。
(2)判断该反应是否达到平衡状态的依据是________________(填序号)。
① CO减少的化学反应速率和CO2减少的化学反应速率相等
② CO、H2O、CO2、H2的浓度都相等
③ CO、H2O、CO2、H2的浓度都不再发生变化
④ 正、逆反应速率都为0
(3)若开始时向该容器中加入CO、H2O(g)、CO2和H2各0.1 mol,在相同条件下,反应达到平衡时,水蒸气的物质的量浓度c(H2O)=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.化学反应实质是旧键断裂新键形成 B.极性键就是共用电子对发生偏移的共价键
C.氢键是一种比较弱的化学键 D.水结冰时体积膨胀、密度减小就是因为氢键的存在
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中能肯定说明金属A比金属B活泼的是
A.A原子最外层电子数比B原子的最外层电子数少
B.A原子电子层数比B原子的电子层数多
C.1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多
D.常温时,A能从酸中置换出氢,而B不能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com