

 $\stackrel{“߻ƼĮ}{”ś}$
$\stackrel{“߻ƼĮ}{”ś}$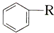 +HCl
+HCl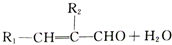
 £®
£® £®
£® £®
£®·ÖĪö ÓÉA”¢BµÄ·Ö×ÓŹ½ÅŠ¶ĻAµ½BµÄ·“Ó¦ŹĒ¼Ó³É·“Ó¦£¬ÓÉB”¢CµÄ·Ö×ÓŹ½æÉÖŖ£¬·“Ó¦ĄąĖĘŅŃÖŖiÖŠČ”“ś·“Ó¦·“Ó¦£¬ÓÉC±»ĖįŠŌøßĆĢĖį¼ŲČÜŅŗŃõ»ÆµÄ²śĪļDµÄ½į¹¹æÉÖŖ£¬CµÄ½į¹¹¼ņŹ½ĪŖ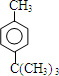 £¬æÉĶĘÖŖAĪŖCH2=C£ØCH3£©2£¬BĪŖ£ØCH3£©3CCl£¬DÓė¼×“¼·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ
£¬æÉĶĘÖŖAĪŖCH2=C£ØCH3£©2£¬BĪŖ£ØCH3£©3CCl£¬DÓė¼×“¼·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ £¬E·¢Éś»¹Ō·“Ó¦µĆF£¬½įŗĻFµÄ·Ö×ÓŹ½æÉÖŖFĪŖ
£¬E·¢Éś»¹Ō·“Ó¦µĆF£¬½įŗĻFµÄ·Ö×ÓŹ½æÉÖŖFĪŖ £¬Fµ½G·¢ÉśĄąĖĘŅŃÖŖiiµÄ·“Ó¦£¬½įŗĻĮåĄ¼Č©µÄ½į¹¹£¬æÉÖŖGµÄ½į¹¹¼ņŹ½ĪŖ
£¬Fµ½G·¢ÉśĄąĖĘŅŃÖŖiiµÄ·“Ó¦£¬½įŗĻĮåĄ¼Č©µÄ½į¹¹£¬æÉÖŖGµÄ½į¹¹¼ņŹ½ĪŖ £¬Gµ½ĮåĄ¼Č©µÄ×Ŗ»ÆÖŠĢ¼Ģ¼Ė«¼ü±»Ļū³ż£¬ŌņGÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHĪŖ
£¬Gµ½ĮåĄ¼Č©µÄ×Ŗ»ÆÖŠĢ¼Ģ¼Ė«¼ü±»Ļū³ż£¬ŌņGÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHĪŖ £¬HŌŁ·¢Éś“ß»ÆŃõ»ÆÉś³ÉĮåĄ¼Č©£¬¾Ż“Ė“šĢā£®
£¬HŌŁ·¢Éś“ß»ÆŃõ»ÆÉś³ÉĮåĄ¼Č©£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗÓÉA”¢BµÄ·Ö×ÓŹ½ÅŠ¶ĻAµ½BµÄ·“Ó¦ŹĒ¼Ó³É·“Ó¦£¬ÓÉB”¢CµÄ·Ö×ÓŹ½æÉÖŖ£¬·“Ó¦ĄąĖĘŅŃÖŖiÖŠČ”“ś·“Ó¦·“Ó¦£¬ÓÉC±»ĖįŠŌøßĆĢĖį¼ŲČÜŅŗŃõ»ÆµÄ²śĪļDµÄ½į¹¹æÉÖŖ£¬CµÄ½į¹¹¼ņŹ½ĪŖ £¬æÉĶĘÖŖAĪŖCH2=C£ØCH3£©2£¬BĪŖ£ØCH3£©3CCl£¬DÓė¼×“¼·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ
£¬æÉĶĘÖŖAĪŖCH2=C£ØCH3£©2£¬BĪŖ£ØCH3£©3CCl£¬DÓė¼×“¼·¢Éśõ„»Æ·“Ӧɜ³ÉEĪŖ £¬E·¢Éś»¹Ō·“Ó¦µĆF£¬½įŗĻFµÄ·Ö×ÓŹ½æÉÖŖFĪŖ
£¬E·¢Éś»¹Ō·“Ó¦µĆF£¬½įŗĻFµÄ·Ö×ÓŹ½æÉÖŖFĪŖ £¬Fµ½G·¢ÉśĄąĖĘŅŃÖŖiiµÄ·“Ó¦£¬½įŗĻĮåĄ¼Č©µÄ½į¹¹£¬æÉÖŖGµÄ½į¹¹¼ņŹ½ĪŖ
£¬Fµ½G·¢ÉśĄąĖĘŅŃÖŖiiµÄ·“Ó¦£¬½įŗĻĮåĄ¼Č©µÄ½į¹¹£¬æÉÖŖGµÄ½į¹¹¼ņŹ½ĪŖ £¬Gµ½ĮåĄ¼Č©µÄ×Ŗ»ÆÖŠĢ¼Ģ¼Ė«¼ü±»Ļū³ż£¬ŌņGÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHĪŖ
£¬Gµ½ĮåĄ¼Č©µÄ×Ŗ»ÆÖŠĢ¼Ģ¼Ė«¼ü±»Ļū³ż£¬ŌņGÓėĒāĘų·¢Éś¼Ó³É·“Ӧɜ³ÉHĪŖ £¬HŌŁ·¢Éś“ß»ÆŃõ»ÆÉś³ÉĮåĄ¼Č©£¬
£¬HŌŁ·¢Éś“ß»ÆŃõ»ÆÉś³ÉĮåĄ¼Č©£¬
£Ø1£©AĪŖCH2=C£ØCH3£©2£¬AµÄ»ÆѧĆū³ĘĪŖ2-¼×»ł-1-±ūĻ©£¬øł¾ŻÉĻĆę·ÖĪöæÉÖŖ£¬ÓÉAÉś³ÉBµÄ·“Ó¦ĄąŠĶĪŖ¼Ó³É·“Ó¦£¬
¹Ź“š°øĪŖ£ŗ2-¼×»ł-1-±ūĻ©£»¼Ó³É·“Ó¦£»
£Ø2£©øł¾ŻÉĻĆę·ÖĪöæÉÖŖ£¬EĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©GµÄ½į¹¹¼ņŹ½ĪŖ £¬G·¢Éś¼Ó¾Ū·“Ó¦µÄ»Æѧ·½³ĢŹ½
£¬G·¢Éś¼Ó¾Ū·“Ó¦µÄ»Æѧ·½³ĢŹ½  £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©HĪŖ £¬H·¢Éś“ß»ÆŃõ»ÆÉś³ÉĮåĄ¼Č©£¬ĖłŅŌÓÉHÉś³ÉĮåĄ¼Č©µÄ·“Ó¦Ģõ¼žĶ»ņŅų”¢¼ÓČČ£¬ŹŌ¼ĮŹĒŃõĘų£¬
£¬H·¢Éś“ß»ÆŃõ»ÆÉś³ÉĮåĄ¼Č©£¬ĖłŅŌÓÉHÉś³ÉĮåĄ¼Č©µÄ·“Ó¦Ģõ¼žĶ»ņŅų”¢¼ÓČČ£¬ŹŌ¼ĮŹĒŃõĘų£¬
¹Ź“š°øĪŖ£ŗĶ»ņŅų”¢¼ÓČČ”¢ŃõĘų£»
£Ø5£©FĪŖ £¬øł¾ŻĢõ¼ža£®±½»·ÉĻµÄÖ»ÓŠĮ½øöČ”“ś»ł£¬ĒŅ“¦ÓŚ¶ŌĪ»£¬b£®ÓöFeCl3ČÜŅŗĻŌ×ĻÉ«£¬ĖµĆ÷ÓŠ·ÓōĒ»ł£¬c£®³ż±½»·ĶāĪŽĘäĖü»·×“½į¹¹£¬Ōņ·ūŗĻĢõ¼žµÄFµÄĶ¬·ÖŅģ¹¹ĢåĪŖ·ÓōĒ»łµÄ¶ŌĪ»ÉĻĮ¬ÓŠĢ¼Į“½į¹¹ĪŖ
£¬øł¾ŻĢõ¼ža£®±½»·ÉĻµÄÖ»ÓŠĮ½øöČ”“ś»ł£¬ĒŅ“¦ÓŚ¶ŌĪ»£¬b£®ÓöFeCl3ČÜŅŗĻŌ×ĻÉ«£¬ĖµĆ÷ÓŠ·ÓōĒ»ł£¬c£®³ż±½»·ĶāĪŽĘäĖü»·×“½į¹¹£¬Ōņ·ūŗĻĢõ¼žµÄFµÄĶ¬·ÖŅģ¹¹ĢåĪŖ·ÓōĒ»łµÄ¶ŌĪ»ÉĻĮ¬ÓŠĢ¼Į“½į¹¹ĪŖ £¬ĖłŅŌ¹²ÓŠ21ÖÖ£¬ĘäÖŠČĪŅāŅ»ÖֵĽį¹¹¼ņŹ½ĪŖ
£¬ĖłŅŌ¹²ÓŠ21ÖÖ£¬ĘäÖŠČĪŅāŅ»ÖֵĽį¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ21£» £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻÓėŗĻ³É£¬³ä·ÖĄūÓĆÓŠ»śĪļµÄ·Ö×ÓŹ½Óė½į¹¹½ųŠŠ·ÖĪö½ā“š£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕ¹ŁÄÜĶŵĊŌÖŹÓė×Ŗ»Æ£¬²ąÖŲæ¼²éѧɜ·ÖĪöĶĘĄķÄÜĮ¦”¢×ŌѧÄÜĮ¦ÓėÖŖŹ¶ĒØŅĘÓ¦ÓĆ£¬ÄѶČÖŠµČ£®


 ĘŚÄ©³å“Ģ100·Ö““ŠĀ½š¾ķĶźČ«ŹŌ¾ķĻµĮŠ“š°ø
ĘŚÄ©³å“Ģ100·Ö““ŠĀ½š¾ķĶźČ«ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½āÖŹČÜŅŗÖŠµē×ÓĻņÕż¼«ŅĘ¶Æ | |
| B£® | ·ÅµēŅ»¶ĪŹ±¼äŗó£¬KOHµÄĪļÖŹµÄĮæÅØ¶Č²»±ä | |
| C£® | ĶØŅŅĶéµÄµē¼«ĪŖøŗ¼« | |
| D£® | ²Ī¼Ó·“Ó¦µÄO2ŗĶC2H6µÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | AÖŠŅ»¶ØÓŠFe2+ | B£® | BĪŖAgI³Įµķ | ||
| C£® | AÖŠæÉÄÜÓŠFe3+ | D£® | AŅ»¶ØĪŖFeBr2ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | V£ØA£©=0.15 mol•L-1•S-1 | B£® | V£ØB£©=0.3 mol•L-1•S-1 | ||
| C£® | V£ØC£©=0.4 mol•L-1•S-1 | D£® | V£ØD£©=0.45 mol•L-1•S-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=12µÄBa£ØOH£©2ČÜŅŗŗĶpH=12µÄNa2CO3ČÜŅŗÖŠ£¬Ė®µēĄėµÄc£ØOH-£©ĻąµČ | |
| B£® | ³£ĪĀĻĀ½«“×ĖįÄĘ”¢ŃĪĖįĮ½ČÜŅŗ»ģŗĻŗó£¬ČÜŅŗ³ŹÖŠŠŌ£¬Ōņ»ģŗĻŗóČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCl-£©£¾c£ØCH3COOH£© | |
| C£® | ³£ĪĀĻĀĪļÖŹµÄĮæÅضČĻąµČµÄ¢ŁNH4HCO3”¢¢ŚNH4HSO4”¢¢ŪNH4Fe£ØSO4£©2£ŗČżÖÖČÜŅŗÖŠNH4+µÄÅØ¶Č£ŗ¢Ś£¾¢Ū£¾¢Ł | |
| D£® | µČĢå»żµČĪļÖŹµÄĮæÅØ¶ČµÄNaClO£Øaq£©ÓėNaCl£Øaq£©ÖŠĄė×Ó×ÜŹż£ŗNĒ°£¾Nŗó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molO2ŗĶ1molH2 | B£® | 5.6LN2£Ø±ź×¼×“æöĻĀ£©ŗĶ11gCO2 | ||
| C£® | 224mLH2£Ø±ź×¼×“æöĻĀ£©ŗĶ0.1molN2 | D£® | 9gH2OŗĶ0.5molBr2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
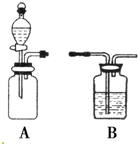 ČēĶ¼ŹĒ֊ѧ»Æѧ֊³£¼ūµÄŹµŃé×°ÖĆ£®
ČēĶ¼ŹĒ֊ѧ»Æѧ֊³£¼ūµÄŹµŃé×°ÖĆ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com