
| A. | 简单氢化物的沸点:Z>W | |
| B. | 由W、Y两种元素形成的化合物一定不含共价键 | |
| C. | 简单气态氢化物的热稳定性:X>W | |
| D. | 元素Y和Z的简单离子具有相同的电子层结构 |
分析 短周期主族W、X、Y、Z的原子序数依次增大,W原子最外层电子数是次外层电子数的3倍,W为O元素;X是迄今发现的非金属性最强的元素,X为F元素;在周期表中Y位于第ⅠA族,结合原子序数可知,Y为Na,Z与W属于同一主族,Z为S元素,以此来解答.
解答 解:由上述分析可知,W为O,X为F,Y为Na,Z为S,
A.水分子间含氢键,沸点高,则简单氢化物的沸点:Z<W,故A错误;
B.W、Y两种元素形成的化合物若为过氧化钠,含离子键、O-O共价键,故B错误;
C.非金属性X>W,则简单气态氢化物的热稳定性:X>W,故C正确;
D.Y和Z的简单离子相差1个电子层,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子结构、元素的性质推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
 5H3AsO4+4Br2+4K2SO4+4H2O.
5H3AsO4+4Br2+4K2SO4+4H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯 | |
| B. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 | |
| C. | 淀粉溶液、豆浆、碳素墨水均可发生丁达尔现象 | |
| D. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -44.2kJ•mol-1 | B. | +44.2kJ•mol-1 | C. | -330kJ•mol-1 | D. | +330kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
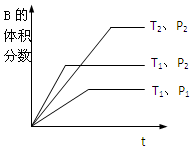 (1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9. 6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
| A. | ①的上层清液中含有Fe2+、Fe3+、Cu2+ | |
| B. | 硝酸的浓度为1mol•L-1 | |
| C. | 每份混合物中铁粉的质量为16.8g | |
| D. | ④中V=11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
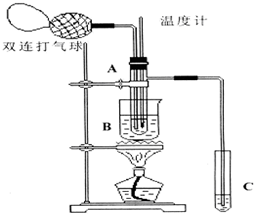 下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.
下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com