
| A. | $\frac{{W}_{x}}{N+x-n}$ mol | B. | $\frac{W(x-n)}{N+x-n}$ mol | C. | $\frac{W(x+n)}{N+x-n}$ mol | D. | $\frac{W(x+n)}{N+x+n}$ mol |
分析 阴离子Rn-的核外电子数为x,则质子数为x-n,R的中子数为N,则质量数为x-n+N,原子中质子数=电子数,结合n=$\frac{m}{M}$计算.
解答 解:阴离子Rn-的核外电子数为x,则质子数为x-n,R的中子数为N,则质量数为x-n+N,
原子中质子数=电子数,则WgR原子中所含电子的物质的量为$\frac{Wg}{(x-n+N)g/mol}$×(x-n)=$\frac{W(x-n)}{N+x-n}$ mol,
故选B.
点评 本题考查物质的量的计算,为高频考点,把握以物质的量为中心的基本计算公式为解答的关键,侧重分析与计算能力的考查,注意原子中数量关系,题目难度不大.


科目:高中化学 来源: 题型:填空题

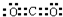 ;写出X、Y之间反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2;
;写出X、Y之间反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮的固定 | |
| B. | 实验室中制取蒸馏水 | |
| C. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集 | |
| D. | 用铂丝蘸取NaCl溶液进行焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲是甲烷,甲烷能使酸性KMnO4溶液褪色 | |
| B. | 乙是乙烯,乙烯可与溴水发生取代反应使溴水褪色 | |
| C. | 丙是苯,苯在空气中燃烧时产生带有浓烟的火焰 | |
| D. | 丁是乙酸,一定条件下乙酸能跟乙醇发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+═H2SiO3↓ | |
| C. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| D. | 向次氯酸钙溶液通入足量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体.
连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com