
减少SO2的排放、回收利用SO2成为世界性的研究课题。我国研究人员研制的利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧废渣产生的SO2制备硫酸锰的生产流程如下:
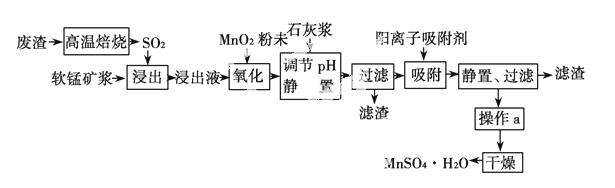
浸出液的pH<2,其中的金属离子主要是 Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。有关金属离子的半径以及形成氢氧化物沉淀时的pH如表所示,阳离子吸附剂吸附金属离子的效
Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。有关金属离子的半径以及形成氢氧化物沉淀时的pH如表所示,阳离子吸附剂吸附金属离子的效 果如图所示。
果如图所示。
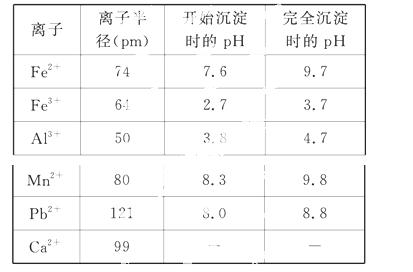
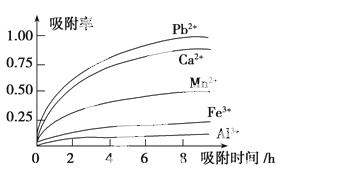
已知PbO2的氧化性大于MnO2的氧化性。请回答下列问题:
(1)废渣的主要成分是硫铁矿,1 mol F eS2高温焙烧转移________ mol电子。
eS2高温焙烧转移________ mol电子。
(2)在氧化后的浸出液中加入石灰浆,用于调节浸出液的pH,pH应调节至________。
(3)阳离子吸附剂用于除去杂质金属离子。决定阳离子吸附剂吸附效果的因素是________(填写序号)。
a.溶液的pH值 b.金属离子的电荷
c.金属离子的半径 d.吸附时间
(4)操作a包括________等过程。
科目:高中化学 来源: 题型:
下列电离方程式错误的是
A.CaCl2 =Ca2++2Cl- B.Ba(OH)2=Ba2++2OH-
C.HNO3=H++NO3- D.NaHCO3=Na++H++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铵溶液中离子浓度关系不正确的是 ( )
A.c(NH )>c(SO
)>c(SO )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(NH )=2c(SO
)=2c(SO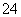 )
)
C.c(NH )+c(NH3·H2O)=2c(SO
)+c(NH3·H2O)=2c(SO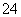 )
)
D.c(NH )+c(H+)=c(OH-)+2c(SO
)+c(H+)=c(OH-)+2c(SO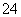 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液中粒子浓度关系的比较中不正确的是 ( )
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.用0.100 0 mol·L-1NaOH溶液滴定未知浓度的CH3COOH溶液,恰好反应时:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.pH=2的HA溶液与pH=12的MOH溶液以任意比混合:
c(H+)+c(M+)=c(OH-)+c(A-)
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,一定量的醋酸与氢氧化钠溶液发生中和反应。下列说法正确的是 ( )
A.当溶液中c(CH3COO-)=c(Na+)时,醋酸与氢氧化钠恰好完全反应
B.当溶液中c(CH3COO-)=c(Na+)时,一定是氢氧化钠过量
C.当溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-)时,一定是醋酸过量
D.当溶液中c(Na+)>c(CH3COO-)>c(OH-) >c(H+)时,一定是氢氧化钠过量
>c(H+)时,一定是氢氧化钠过量
查看答案和解析>>
科目:高中化学 来源: 题型:
化学 中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
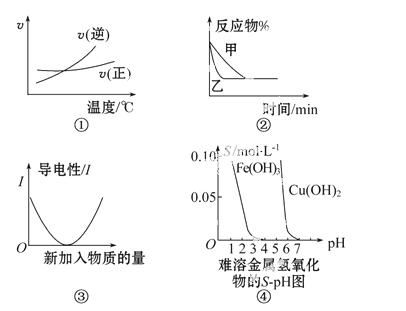
A.根据图①可判断可逆反应A2(g)+3B2(g)  2AB3(g),正反应是吸热反应
2AB3(g),正反应是吸热反应
B.图②表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图④溶解度与溶液pH的关系,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO,至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,N2O分解的部分实验数据如下:
| 反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| c(N2O)/mol/L | 0.1 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
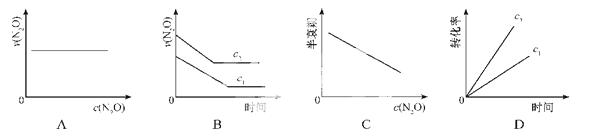
下图能正确表示该反应有关物理量变化规律的是
(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1<c2)
查看答案和解析>>
科目:高中化学 来源: 题型:
丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/mL,沸点约55 oC,分离水和丙酮时最合理的方法是:
A. 蒸发 B. 分液 C.过滤 D. 蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
Li﹣Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e﹣=Li2S+Fe.有关该电池的下列说法中,正确的是( )
|
| A. | Li﹣Al在电池中作为负极材料,该材料中Li的化合价为+1价 |
|
| B. | 该电池的电池反应式为:2Li+FeS=Li2S+Fe |
|
| C. | 负极的电极反应式为Al﹣3e﹣=Al3+ |
|
| D. | 充电时,阴极发生的电极反应式为:Li2S+Fe﹣2e﹣=2Li++FeS |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com