
¶ž¼×ĆŃ£ØCH3OCH3£©ŹĒŅ»ÖÖŠĀŠĶµÄŗĻ³É”°²ńÓĶ”±”£ĖüæÉÓÉÉśĪļ¼×Ķé»ņĢģČ»ĘųŗĻ³É”£
¢ÅÉśĪļ¼×ĶéŹĒÓÉÖ²ĪļŗĶ¶ÆĪļ·ą±ćŌŚŅ»¶ØĢõ¼žĻĀ·¢½Ķ¶ųµĆµÄ¼×Ķé£ŗ
![]()
ČōijֲĪļĻĖĪ¬ĖŲµÄŗ¬ĮæĪŖ10%£¬Ä³ÕÓĘų³Ų£¬µ±¼ÓČėøĆÖ²Īļ162kg£¬ŌŚĪ¢ÉśĪļ×÷ÓĆĻĀĶźČ«×Ŗ»ÆæɵĆCH4ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ m3”£
¢ĘŗĻ³É¶ž¼×ĆŃÖ÷ŅŖ²½ÖčĪŖŌģĘųŗĶŗĻ³É”£¹ż³ĢČēĻĀ£ŗ
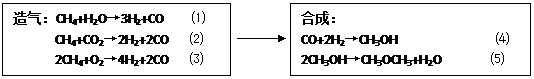 |
ČōŌģĘųŹ±£¬ÉčĆæ²½×Ŗ»ÆĀŹ¾łĪŖ100%£¬ÉčijĢģČ»ĘųÖŠÖ»ŗ¬5%CO2£¬²»ŗ¬ĘäĖūŌÓÖŹ£¬Ćæ100m3ĢģČ»Ęų£¬Ó¦Ķ¬Ź±ĶØČėĖ®ÕōĘųŗĶæÕĘųø÷¶ąÉŁĢå»ż£ØæÕĘųÖ»ŗ¬N2ŗĶO2£¬ĒŅĢå»ż±ČĪŖ4£ŗ1£¬ĻĀĶ¬£©£¬²ÅÄܱ£Ö¤ŗĻ³ÉŹ±COŗĶH2³ä·ÖĄūÓĆ”£V[H2O£Øg£©]= m3£»V[æÕĘų]= m3”£
¢ĒĪŖĮĖ³ä·ÖĄūÓĆ·“Ó¦¹ż³ĢÖŠÉś³ÉµÄ±Č½Ļ“æ¾»µÄµŖĘų£¬Ä³ĘóŅµÓĆĢģČ»ĘųĪŖÖ÷ŅŖŌĮĻĮŖŗĻÉś²ś¶ž¼×ĆŃŗĶ°±£¬¹ż³ĢČēĻĀ£ŗ
ÖĘĘųÉč±ø£ŗ¢ŁCH4+H2O ”ś CO+3H2 ¢Ś2CH4+O2 ”ś 2CO+4H2
ŗĻ³ÉĖž¢ń£ŗCO+2H2 ”ś CH3OH £» 2CH3OH ”ś CH3OCH3+H2O
ŗĻ³ÉĖž¢ņ£ŗN2+3H2==2NH3
¼ŁÉčĢģČ»ĘųÖŠÖ»ŗ¬CH4£¬·“Ó¦¢ŚÖŠĶØČėŹŹĮææÕĘų£¬µ÷½Ś¢ŁŗĶ¢ŚĶ¶ČėµÄCH4µÄĮ棬ŅŌŹ¹·“Ó¦¢ŁŹ£ÓąµÄH2ŗĶ·“Ó¦¢ŚŹ£ÓąµÄN2µÄĢå»ż±ČĒ”ŗĆĪŖ3£ŗ1£¬ŅŌ±ćŗĻ³É°±”£øĆĘóŅµĆæÉś²ś34t NH3ĄķĀŪÉĻĶ¬Ź±æÉŅŌµĆµ½¶ž¼×ĆѶąÉŁ¶Ö£æ£ØÉč¹¤Ņµ¶ą“Ī×Ŗ»Æ£¬×Ü×Ŗ»ÆĀŹ¼Ł¶ØĪŖ100%ÉčŗĻ³ÉĖž¢ńÖŠĖ®ÓėCO²»·“Ó¦£©£æ
£Ø1£©6.72m3 (2·Ö) (2)10m3,200m3 (ĆææÕ2·Ö) (3)80.5t (4·Ö)
±¾Ģāæ¼²é¶ą²½·“Ó¦µÄ»Æѧ¼ĘĖć£¬¹ŲĻµø“ŌÓ£¬ÄŃ¶Č½Ļ“ó£¬ČŻŅ׳ö“ķ£¬ŹĒŅ»µĄæ¼²é×ŪŗĻĖ¼Ī¬ÄÜĮ¦”¢Ēų·Ö¶ČŗƵďŌĢā”£(1)(C6H10O5) n ~ 3nCH4,¼“C6H10O5 ~ 3CH4
n(CH4)=3n(C6H10O5) =![]()
V(CH4)=300mol”Į22.4L/mol=6.72”Į103L=6.72m3
(2)ŅĄĢāŅā£¬100m3ĢģČ»Ęųŗ¬CH495m3”¢CO25m3”£¹Ū²ģŗĻ³É·“Ó¦£¬CO:H2=1:2Ź±²ÅÄܳä·ÖĄūÓĆ”£ŌŁ¹Ū²ģŌģĘų·“Ó¦£¬·“Ó¦£Ø1£©±ŲŠėŹĒ£Ø2£©µÄ2±¶²ÅÄÜ“ļµ½ÉĻŹöŅŖĒó”£ÓÖÖŖ·“Ó¦£Ø2£©ŗÄCH4ĪŖ5m3£¬Ōņ·“Ó¦£Ø1£©ŗÄCH4ĪŖ10m3£¬Ķ¬Ź±ŠčĖ®10m3£»ĖłŅŌ·“Ó¦£Ø3£©µÄCH4ĪŖ80m3£¬ŠčO240m3£¬¼“æÕĘų200m3”£
£Ø3£©ÓÉ·“Ó¦N2+3H2==2NH3æÉĒóµĆÉś²ś34t°±Šč1”Į106molN2ŗĶ3”Į106molH2£¬Ōņ·“Ó¦¢ŚĶØČėµÄO2ĪŖ1”Į1/4=0.25”Į106mol£¬Éś³ÉH21”Į106mol£»Ōņ·“Ó¦¢ŁÓ¦Éś³ÉH29”Į106mol£¬ĘäÖŠÓĆÓŚŗĻ³ÉCH3OCH3µÄH2ĪŖ6”Į106mol£¬ÓɹŲĻµŹ½4H2 ~ CH3OCH3æÉĒóµĆ£ŗn(CH3OCH3)=£Ø1”Į106+6”Į106£©mol”Į1/4=1.75”Į106mol£¬ĪŖ80.5t”£


 Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ĪļÖŹ | CH3OH | CH3OCH3 | H2O |
| ÅضČ/£Ømol?L-1£© | 0.28 | 0.86 | 0.86 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ½ĖÕŹ”ĪŽĪżŹŠøßČżÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
£Ø14·Ö£©¶ž¼×ĆŃ£ØCH3OCH”££©ŗĶ¼×“¼£ØCH3OH£©±»³ĘĪŖ21ŹĄ¼ĶµÄŠĀŠĶČ¼ĮĻ£¬¾ßÓŠĒå½ą”¢øߊ§µČÓÅĮ¼µÄŠŌÄÜ”£ŅŌCH4ŗĶH2OĪŖŌĮĻÖʱø¶ž¼×ĆŃŗĶ¼×“¼µÄ¹¤ŅµĮ÷³ĢČēĻĀ£ŗ

£Ø1£©“߻Ʒ“Ó¦ŹŅBÖŠCOÓėH2ŗĻ³É¶ž¼×ĆѵĻÆѧ·½³ĢŹ½ĪŖ .
£Ø2£©“߻Ʒ“Ó¦ŹŅAÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CH4£Øg£©+H2O£Øg£© CO£Øg£©+3H2£Øg£©””£ØI£©”¢CO£Øg£©+H2O£Øg£©
CO£Øg£©+3H2£Øg£©””£ØI£©”¢CO£Øg£©+H2O£Øg£© CO2£Øg£©+H2£Øg£©””£Ø¢ņ£©“߻Ʒ“Ó¦ŹŅCÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CO2£Øg£©+H2£Øg£©””£Ø¢ņ£©“߻Ʒ“Ó¦ŹŅCÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CO£Øg£©+2H2£Øg£© CH3OH£Øg£©””£Ø¢ó£©”¢CO2£Øg£©+3H2£Øg£©
CH3OH£Øg£©””£Ø¢ó£©”¢CO2£Øg£©+3H2£Øg£© CH3OH£Øg£©+H2O£Øg£©””£Ø¢ō£©
CH3OH£Øg£©+H2O£Øg£©””£Ø¢ō£©
¢ŁŅŃÖŖ£ŗŌ×ÓĄūÓĆĀŹ= ”Į100£„£¬ŹŌĒó·“Ó¦£Ø¢ō£©µÄŌ×ÓĄūÓĆĀŹĪŖ ”£
”Į100£„£¬ŹŌĒó·“Ó¦£Ø¢ō£©µÄŌ×ÓĄūÓĆĀŹĪŖ ”£
¢Ś·“Ó¦£Ø¢ō£©µÄ”÷S 0£ØĢī”°>”±”¢”°=”±»ņ”°<”±£©”£
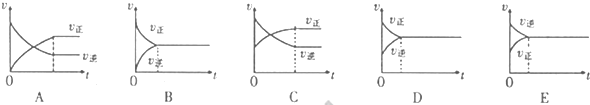
¢ŪŌŚŃ¹ĒæĪŖ5MPa£¬Ģå»żĪŖVLµÄ·“Ó¦ŹŅcÖŠ£¬amol COÓė20mol H2ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£Ø¢ó£©Éś³É¼×“¼£¬COµÄ×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµČēÓŅĶ¼”£ŌņøĆ·“Ó¦µÄ”÷H 0£ØĢī”°>”±”¢”°=”±»ņ”°<”±£©”£300”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK= £ØÓĆŗ¬×ÖÄøµÄ“śŹżŹ½±ķŹ¾£©”£

£Ø3£©ĪŅ¹śÄ³æĘŃŠĖłĢį¹©Ņ»ÖÖ¼īŠŌ”°Ö±½Ó¶ž¼×ĆŃČ¼ĮĻµē³Ų”±”£
øĆČ¼ĮĻµē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ
CH3OCH3Ņ»12eŅ»+16OHŅ»=2CO2-3+11H2O”£ÓŠČĖĢį³öĮĖŅ»ÖÖĄūÓĆĀČ¼ī¹¤Ņµ²śĘ·ÖĪĄķŗ¬¶žŃõ»ÆĮņ£ØĢå»ż·ÖŹżĪŖx£©·ĻĘųµÄ·½·ØČēĻĀ£ŗ
¢Ł½«ŗ¬SO2µÄ·ĻĘųĶØČĖµē½ā±„ŗĶŹ³ŃĪĖ®ĖłµĆČÜŅŗÖŠ£¬µĆNaHSO3ČÜŅŗ£»
¢Ś½«µē½ā±„ŗĶŹ³ŃĪĖ®ĖłµĆĘųĢå·“Ó¦ŗóÖʵĆŃĪĖį£»
¢Ū½«ŃĪĖį¼ÓČėNaHSO3ČÜŅŗÖŠµĆSO2ĘųĢå»ŲŹÕ”£
ÓĆÉĻŹö¼īŠŌ”°Ö±½Ó¶ž¼×ĆŃČ¼ĮĻµē³Ų”±µē½āŹ³ŃĪĖ®Ą““¦Ąķ±ź×¼×“æöĻĀVLµÄ·ĻĘų£¬¼ĘĖćĻūŗĶž¼×ĆѵÄÖŹĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø14·Ö£©¶ž¼×ĆŃ£ØCH3OCH”££©ŗĶ¼×“¼£ØCH3OH£©±»³ĘĪŖ21ŹĄ¼ĶµÄŠĀŠĶČ¼ĮĻ£¬¾ßÓŠĒå½ą”¢øߊ§µČÓÅĮ¼µÄŠŌÄÜ”£ŅŌCH4ŗĶH2OĪŖŌĮĻÖʱø¶ž¼×ĆŃŗĶ¼×“¼µÄ¹¤ŅµĮ÷³ĢČēĻĀ£ŗ
£Ø1£©“߻Ʒ“Ó¦ŹŅBÖŠCOÓėH2ŗĻ³É¶ž¼×ĆѵĻÆѧ·½³ĢŹ½ĪŖ .
£Ø2£©“߻Ʒ“Ó¦ŹŅAÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CH4£Øg£©+H2O£Øg£©![]() CO£Øg£©+3H2£Øg£©””£ØI£©”¢CO£Øg£©+H2O£Øg£©
CO£Øg£©+3H2£Øg£©””£ØI£©”¢CO£Øg£©+H2O£Øg£©![]() CO2£Øg£©+H2£Øg£©””£Ø¢ņ£©“߻Ʒ“Ó¦ŹŅCÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CO2£Øg£©+H2£Øg£©””£Ø¢ņ£©“߻Ʒ“Ó¦ŹŅCÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CO£Øg£©+2H2£Øg£©![]() CH3OH£Øg£©””£Ø¢ó£©”¢CO2£Øg£©+3H2£Øg£©
CH3OH£Øg£©””£Ø¢ó£©”¢CO2£Øg£©+3H2£Øg£©![]() CH3OH£Øg£©+H2O£Øg£©””£Ø¢ō£©
CH3OH£Øg£©+H2O£Øg£©””£Ø¢ō£©
¢ŁŅŃÖŖ£ŗŌ×ÓĄūÓĆĀŹ= ”Į100£„£¬ŹŌĒó·“Ó¦£Ø¢ō£©µÄŌ×ÓĄūÓĆĀŹĪŖ ”£
”Į100£„£¬ŹŌĒó·“Ó¦£Ø¢ō£©µÄŌ×ÓĄūÓĆĀŹĪŖ ”£
¢Ś·“Ó¦£Ø¢ō£©µÄ”÷S 0£ØĢī”°>”±”¢”°=”±»ņ”°<”±£©”£
¢ŪŌŚŃ¹ĒæĪŖ5MPa£¬Ģå»żĪŖVLµÄ·“Ó¦ŹŅcÖŠ£¬amol COÓė20mol H2ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£Ø¢ó£©Éś³É¼×“¼£¬COµÄ×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµČēÓŅĶ¼”£ŌņøĆ·“Ó¦µÄ”÷H 0£ØĢī”°>”±”¢”°=”±»ņ”°<”±£©”£300”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK= £ØÓĆŗ¬×ÖÄøµÄ“śŹżŹ½±ķŹ¾£©”£
£Ø3£©ĪŅ¹śÄ³æĘŃŠĖłĢį¹©Ņ»ÖÖ¼īŠŌ”°Ö±½Ó¶ž¼×ĆŃČ¼ĮĻµē³Ų”±”£
øĆČ¼ĮĻµē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ
CH3OCH3Ņ»12eŅ»+16OHŅ»=2CO2-3+11H2O”£ÓŠČĖĢį³öĮĖŅ»ÖÖĄūÓĆĀČ¼ī¹¤Ņµ²śĘ·ÖĪĄķŗ¬¶žŃõ»ÆĮņ£ØĢå»ż·ÖŹżĪŖx£©·ĻĘųµÄ·½·ØČēĻĀ£ŗ
¢Ł½«ŗ¬SO2µÄ·ĻĘųĶØČĖµē½ā±„ŗĶŹ³ŃĪĖ®ĖłµĆČÜŅŗÖŠ£¬µĆNaHSO3ČÜŅŗ£»
¢Ś½«µē½ā±„ŗĶŹ³ŃĪĖ®ĖłµĆĘųĢå·“Ó¦ŗóÖʵĆŃĪĖį£»
¢Ū½«ŃĪĖį¼ÓČėNaHSO3ČÜŅŗÖŠµĆSO2ĘųĢå»ŲŹÕ”£
ÓĆÉĻŹö¼īŠŌ”°Ö±½Ó¶ž¼×ĆŃČ¼ĮĻµē³Ų”±µē½āŹ³ŃĪĖ®Ą““¦Ąķ±ź×¼×“æöĻĀVLµÄ·ĻĘų£¬¼ĘĖćĻūŗĶž¼×ĆѵÄÖŹĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012½ģ½ĖÕŹ”ĪŽĪżŹŠøßČżÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
£Ø14·Ö£©¶ž¼×ĆŃ£ØCH3OCH”££©ŗĶ¼×“¼£ØCH3OH£©±»³ĘĪŖ21ŹĄ¼ĶµÄŠĀŠĶČ¼ĮĻ£¬¾ßÓŠĒå½ą”¢øߊ§µČÓÅĮ¼µÄŠŌÄÜ”£ŅŌCH4ŗĶH2OĪŖŌĮĻÖʱø¶ž¼×ĆŃŗĶ¼×“¼µÄ¹¤ŅµĮ÷³ĢČēĻĀ£ŗ
£Ø1£©“߻Ʒ“Ó¦ŹŅBÖŠCO ÓėH2ŗĻ³É¶ž¼×ĆѵĻÆѧ·½³ĢŹ½ĪŖ .
ÓėH2ŗĻ³É¶ž¼×ĆѵĻÆѧ·½³ĢŹ½ĪŖ .
£Ø2£©“߻Ʒ“Ó¦ŹŅAÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CH4£Øg£©+H2O£Øg£© CO£Øg£©+3H2£Øg£©””£ØI£©”¢CO£Øg£©+H2O£Øg£©
CO£Øg£©+3H2£Øg£©””£ØI£©”¢CO£Øg£©+H2O£Øg£© CO2£Øg£©+H2£Øg£©””£Ø¢ņ£©“߻Ʒ“Ó¦ŹŅCÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CO2£Øg£©+H2£Øg£©””£Ø¢ņ£©“߻Ʒ“Ó¦ŹŅCÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
CO£Øg£©+2H2£Øg£© CH3OH£Øg£©””£Ø¢ó£©”¢CO2£Øg£©+3H2£Øg£©
CH3OH£Øg£©””£Ø¢ó£©”¢CO2£Øg£©+3H2£Øg£© CH3OH£Øg£©+H2O£Øg£©””£Ø¢ō£©
CH3OH£Øg£©+H2O£Øg£©””£Ø¢ō£©
¢ŁŅŃÖŖ£ŗŌ×ÓĄūÓĆĀŹ= ”Į100£„£¬ŹŌĒó·“Ó¦£Ø¢ō£©µÄŌ×ÓĄūÓĆĀŹĪŖ ”£
”Į100£„£¬ŹŌĒó·“Ó¦£Ø¢ō£©µÄŌ×ÓĄūÓĆĀŹĪŖ ”£
¢Ś·“Ó¦£Ø¢ō£©µÄ”÷S 0£ØĢī”°>”±”¢”°=”±»ņ”°<”±£©”£
¢ŪŌŚŃ¹ĒæĪŖ5MPa£¬Ģå»żĪŖVLµÄ·“Ó¦ŹŅcÖŠ£¬amol COÓė20mol H2ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£Ø¢ó£©Éś³É¼×“¼£¬COµÄ×Ŗ»ÆĀŹÓėĪĀ¶ČµÄ¹ŲĻµČēÓŅĶ¼”£ŌņøĆ·“Ó¦µÄ”÷H 0£ØĢī”°>”±”¢”°=”±»ņ”°<”±£©”£300”ꏱøĆ·“Ó¦µÄĘ½ŗā³£ŹżK= £ØÓĆŗ¬×ÖÄøµÄ“śŹżŹ½±ķŹ¾£©”£
£Ø3£©ĪŅ¹śÄ³æĘŃŠĖłĢį¹©Ņ»ÖÖ¼īŠŌ”°Ö±½Ó¶ž¼×ĆŃČ¼ĮĻµē³Ų”±”£
øĆČ¼ĮĻµē³Ųøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ
CH3OCH3Ņ»12eŅ»+16OHŅ»=2CO2-3+11H2O”£ÓŠČĖĢį³öĮĖŅ»ÖÖĄūÓĆĀČ¼ī¹¤Ņµ²śĘ·ÖĪĄķŗ¬¶žŃõ»ÆĮņ£ØĢå»ż·ÖŹżĪŖx£©·ĻĘųµÄ·½·ØČēĻĀ£ŗ
¢Ł½«ŗ¬SO2µÄ·ĻĘųĶØČĖµē½ā±„ŗĶŹ³ŃĪĖ®ĖłµĆČÜŅŗÖŠ£¬µĆNaHSO3ČÜŅŗ£»
¢Ś½«µē½ā±„ŗĶŹ³ŃĪĖ®ĖłµĆĘųĢå·“Ó¦ŗóÖʵĆŃĪĖį£»
¢Ū½«ŃĪĖį¼ÓČėNaHSO3ČÜŅŗÖŠµĆSO2ĘųĢå»Ų ŹÕ”£
ŹÕ”£
ÓĆÉĻŹö¼īŠŌ”°Ö±½Ó¶ž¼×ĆŃČ¼ĮĻµē³Ų”±µē½āŹ³ŃĪĖ®Ą““¦Ąķ±ź×¼×“æöĻĀVLµÄ·ĻĘų£¬¼ĘĖćĻūŗĶž¼×ĆѵÄÖŹĮ攣
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com