

| A. | 有机物甲中共有两种化学环境下的氢 | |
| B. | 紫草宁的分子式为C16H18O5 | |
| C. | 紫草宁有8个不饱和度 | |
| D. | 在一定条件下,紫草宁可以发生氧化反应、还原反应、取代反应、加聚反应 |
分析 A、根据对称性原则确定有机物中的等效氢原子数目;
B、根据结构简式书写分子式;
C、1个碳碳双键的不饱和度为1,1个碳环的不饱和度为1,碳碳三键的不饱和度为2,据此结合该有机物的结构简式计算其不饱和度;
D、根据有机物具有的官能团确定有机物的性质.
解答 解:A、根据对称性原则,可以确定有机物中的等效氢原子数目是2,所以有机物甲中共有两种化学环境下的氢,故A正确;
B、根据结构简式,得到有机物的分子式C16H16O5,故B错误;
C、1个碳碳双键的不饱和度为1,1个碳环的不饱和度为1,碳碳三键的不饱和度为2,据此得到该有机物的不饱和度是7,故C错误;
D、有机物具有的官能团:酚羟基、醇羟基和羰基,确定有机物的性质可以发生氧化反应、还原反应、取代反应、加聚反应,故D正确.
故选AD.
点评 本题考查学生有机物的结构和性质知识,注意官能团和有机物的结构和性质之间的关系是关键,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
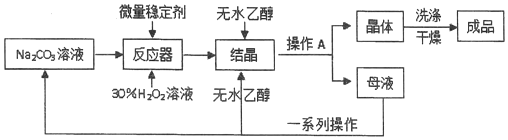
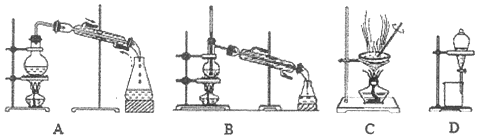

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层的电子数随核电荷数的增加而增多 | |
| B. | 单质颜色随核电荷数的增加而加深 | |
| C. | 氢化物的稳定性随核电荷数的增加而减弱 | |
| D. | 非金属性随核电荷数的增加而减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

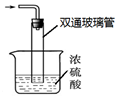
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com