
100 mL 6 mol·L-1H2SO?4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的 ( )
A.Na2CO3固体 B.NaCl溶液 C.浓H2SO4 D.KNO3溶液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )

A.两个装置之间没有盐桥,故不能形成电流
B.a电极的电极反应式:C2H5OH+16OH--12e-===2CO +11H2O
+11H2O
C.一段时间后,乙池d电极周围的溶液呈现棕褐色
D.乙池在反应前后溶液的pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
可充电电池因其可以反复使用而深受广大消费者喜爱。请你根据对可充电电池的理解,选出下列有关说法正确的是 ( )
A.放电时,正极发生氧化反应 B.放电时,把热能转化为电能
C.充电时,电池的负极发生还原反应 D.充电时,把化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.在t℃时,某NaOH稀溶液中,c(H+)=10-a mol/L,c(OH-)=10-b mol/L,
已知a+b=12,则:
该温度下,水的离子积常数Kw= 。
‚该温度下,将10mL 0.1mol/L的稀硫酸与10mL 0.4mol/L的NaOH溶液混合后,溶液的pH= ,此时该溶液中由水电离的c(OH-)= mol/L。(忽略体积变化)
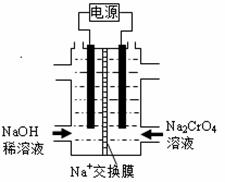
Ⅱ. 根据2CrO42-(黄)+2H+ =====Cr2O72-(橙)+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,电解一段时间后,右边溶液逐渐由黄色变为橙色。图中右侧电极连接电源的 极,其电极反应式为
,通电完成后,若转移0.1mol电子,则阴极区和阳极区的质量差为 g。(已知电解前两极区溶液质量相同)
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X的最高正价和负价的绝对值之差为6,元素Y原子次外层与元素X原子次外层均为8个电子,X、Y的离子具有相同的电子排布,X、Y形成的化合物是( )
A.MgF2 B.MgCl2 C.CaCl2 D.CaBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E为原子序数依次增大的短周期元素。已知A、B、E三种原子最外层共有11个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应生成盐和水;C元素的最外层电子数比次外层电子数少4,D元素的最高正价与最低负价的代数和为4。
请回答下列问题:
(1)元素C在元素周期表中的位置是 ,元素D是 (填元素符号)。元素E是 (填名称),五种元素中离子半径最小的是 (写离子符号)。
(2)C, D, E三种元素最高价氧化物对应水化物的酸性由强到弱的顺序
为 (填化学式)。
(3)写出A和E两元素与最高价氧化物对应水化物反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是
A. ⅦA族元素是同周期中非金属性最强的元素
B. 原子序数为15的元素的最高化合价为+3
C.第二周期ⅣA族元素的原子核电荷数和中子数一定为6
D.原子序数为52的元素位于元素周期表的第五周期ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:B ,C ,D
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
。
(3)写出A、B两元素的最高价氧化物的水化物相互反应的离子方程式:
。
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示) 。
(5)D、E两元素形成化合物属 (“离子”或“共价”)化合物。其中D显最高价的化合物与水反应能生成两种酸,写出其反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.(新课标全国高考)常温常压下,22.4 L氯气与足量镁粉充分反应,转移的电子数为2NA
B.(山东高考)化合反应均为氧化还原反应
C.(山东高考)电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数)
D.(福建高考)易燃试剂与强氧化性试剂分开放置并远离火源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com