
【题目】现有常见金属A存在如下的转化关系(图中有些反应的产物和条件没有全部标出),其中E为白色沉淀。
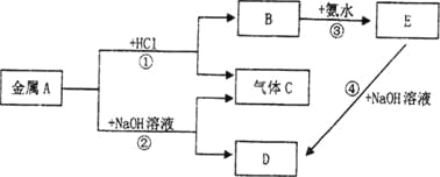
请回答下列问题:
(1) A的化学式为______________。
(2) C的电子式为_________________。
(3) 反应③的化学方程式为_________________________。
(4) 反应④的离子方程式为__________________________。
【答案】(1)Al(1分)(2)H:H(1分)
(3)A1Cl3+3NH3H2O=Al(OH)3↓+3NH4CI(2分)
(4)A1(OH)3+OH-==A1O2-+2H2O(2分)
【解析】
试题分析:金属A既能与盐酸反应,也能与氢氧化钠溶液生成气体C,所以A是铝,B是氯化铝,C是氢气,D是偏铝酸钠,氯化铝和氨水反应生成氢氧化铝沉淀,氢氧化铝溶解在氢氧化钠中生成偏铝酸钠。
(1)根据以上分析可知A的化学式为Al;
(2)氢气的电子式为H:H;
(3)氯化铝和氨水反应的化学方程式为A1Cl3 + 3NH3 H2O = Al(OH)3↓+ 3NH4Cl;
(4)氢氧化铝和氢氧化钠溶液反应的离子方程式为A1(OH)3+OH-==A1O2-+2H2O。


科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是
A.甲烷的标准燃烧热为890.3 kJ·mol1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol1
CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol1
B.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g)ΔH=-38.6 kJ·mol1
2NH3(g)ΔH=-38.6 kJ·mol1
C.S(s)+O2(g)=SO2(g) ΔH=-269.8 kJ·mol1
D.2NO2=O2+2NO ΔH=+116.2 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

下列说法中正确的是
A.1molN2(g)和1molO2(g)完全反应放出的能量为180kJ
B.通常情况下,N2(g)和O2(g)混合能直接生成NO
C.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素,A、B、C三种元素的原子序数之和为31,D元素与A、B、C三种元素既不同周期,也不同主族,请回答:
(1)C元素在元素周期表中的位置是_____________________________;
(2)A、B、D可组成一种离子化合物,是常见的化肥,其化学式为_________________;
(3)A2和D2两种物质可以构成一种新型的原电池,若原电池中电解质溶液为KOH溶液,则正极的电极反应式为_____________________________;
(4)若将一充满20 mlBA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下,测得试管中余下5mL无色气体,则原混合气体中BA2和A2物质的量之比为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科学、技术、社会、环境密切相关。下列有关说法中正确的是( )
A. 节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
B. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰
C. 化学药品着火,都要立即用水或泡沫灭火器灭火
D. PM2.5中含有铅、铬、钒、砷等对人体有害的金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2 moI·L-l的Na2CO3溶液与0.2 moI·L-l的盐酸等体积混合后,所得溶液中部分微粒组分与浓度的关系如图所示,X、Y、Z均表示含碳微粒,下列说法正确的是

A. A代表Na+浓度
B. 该溶液中c(OH-)>c(Y)
C. 向该溶液中加水稀释,所有离子浓度均减小
D. 该混合溶液中:c(X)+c(Y)+c(Z)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
(2)以甲烷为原料可制得氢气。图1是一定温度、压强下,CH4(g)与H2O(g)反应生成CO(g)和1mol H2(g)的能量(KJ)变化示意图,写出该反应的热化学方程式_______________(△H用E1、E2、E3表示)。

(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)![]() MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
A.容器内气体压强保持不变
B.吸收y mol H2只需1 mol MHx
C.若降温,该反应的平衡常数增大
D.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-![]() FeO42-+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
FeO42-+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。

①电解一段时间后,c(OH-)降低的区域在__________(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_____________。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,分析N点c( Na2FeO4)低于最高值的原因:_____________。
(5)在容积可变的密闭容器中充入10molCO和20molH2,发生CO ( g ) + 2H2 ( g )![]() CH3OH ( g ) △H<0, CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为1 L。若反应开始时仍充入10mol CO 和20mol H2,则在平衡状态B时容器的体积V(B)= L。
CH3OH ( g ) △H<0, CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为1 L。若反应开始时仍充入10mol CO 和20mol H2,则在平衡状态B时容器的体积V(B)= L。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. CO燃烧是放热反应 B. H2SO4与NaOH反应是放热反应
C. CaO与H2O反应是吸热反应 D. CaCO3受热分解是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产密切相关。下列说法正确的是( )
A. 硫酸铁净水的原理和漂白粉消毒的原理相同
B. 汽车尾气中的氮氧化物是汽油不完全燃烧造成的
C. 研制高性能的耐磨轮胎,可减少PM2.5等细颗粒物的产生
D. 应用高纯度单质硅制成光导纤维,可提高信息传输速度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com