
 NaCNΪ�綾���ij��ѧ��ȤС��������ϵ�֪��ʵ��������軯����Һ��ʹ�������������Һ����ͳһ�ⶾ���٣����ǿ�չ����������ʵ�飬����Ҫ��ش����⣺
NaCNΪ�綾���ij��ѧ��ȤС��������ϵ�֪��ʵ��������軯����Һ��ʹ�������������Һ����ͳһ�ⶾ���٣����ǿ�չ����������ʵ�飬����Ҫ��ش����⣺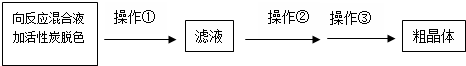
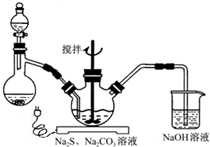
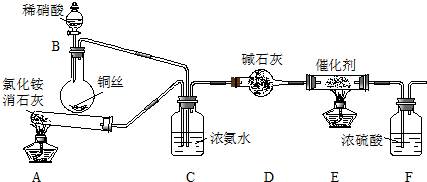
���� ��1�����������ơ����ƺ�̼���Ƶ�Ϊԭ�ϡ���������װ���Ʊ���������ƣ����ݷ�Ӧԭ����֪��������ƿ�м������Ҫʹ��Ӧ���ֽϿ�ķ�Ӧ���ʣ�Ũ���ᡢ���ᶼ�ӷ�����ϡ������룬��Ӧ���ʽ��������������ṩ����Ϣ��֪��Na2S ��Na2CO3�ķ�Ӧ����ʽΪ2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2���ݴ˴��⣻
��2���������⣬Na2S2O3�����������»�����S������Һ��pH�ӽ���С��7ʱ�����SO2ͨ������������NaHSO3���ݴ���д��ѧ����ʽ��
��3����������������Һ�л�ýϸ߲���Na2S2O3?5H2O���ڻ��Һ�м������̼��ɫ��Ȼ����ȹ��ˣ���ֹ��Һ��Na2S2O3?5H2O����������ȥ̼�����Һ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����ɵô־��壬�ݴ˴��⣻
��Ʒ���ȵļ��
��1��vmL0.010mol/L��ˮ��Һ��n��I2��=v��10-3L��0.010mol/L=v��10-5mol�����ݹ�ϵʽ2Na2 S2O3��I2���� mg��Ʒ��n��Na2 S2O3��������m=nM����mg��Ʒ��Na2 S2O3•5H2O������������ݴ˾ݴ˴��ȣ�
��������ʵ�������֪�����ɵ���Һ��ʹ FeCl3��Һ����Ѫ��ɫ��˵����SCN-���������ݵ���غ��Ԫ���غ����д���ӷ���ʽ��
��� �⣺��1�����������ơ����ƺ�̼���Ƶ�Ϊԭ�ϡ���������װ���Ʊ���������ƣ����ݷ�Ӧԭ����֪��������ƿ�м������Ҫʹ��Ӧ���ֽϿ�ķ�Ӧ���ʣ�Ũ���ᡢ���ᶼ�ӷ�����ϡ������룬��Ӧ���ʽ�����������70%�����ᣬѡC�����������ṩ����Ϣ��֪��Na2S ��Na2CO3�ķ�Ӧ����ʽΪ2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2������Na2S ��Na2CO3��������ʵ�������2��1��
�ʴ�Ϊ��C��2��1��
��2���������⣬Na2S2O3�����������»�����S������Һ��pH�ӽ���С��7ʱ�����SO2ͨ������������NaHSO3����Ӧ�Ļ�ѧ����ʽΪNa2S2O3+SO2+H2O=2NaHSO3+S����
�ʴ�Ϊ��Na2S2O3+SO2+H2O=2NaHSO3+S����
��3����������������Һ�л�ýϸ߲���Na2S2O3?5H2O���ڻ��Һ�м������̼��ɫ��Ȼ����ȹ��ˣ���ֹ��Һ��Na2S2O3?5H2O����������ȥ̼�����Һ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����ɵô־��壬���Բ����ٳ��ȹ��ˣ���Ŀ���ǣ�������Ϊ�˷�ֹ�����ڹ��˵Ĺ�������©�����������²��ʽ��ͣ�������Ϊ�˳�ȥ����̿����Ȳ��������ʣ�������������Ũ������ȴ�ᾧ��
�ʴ�Ϊ��������Ϊ�˷�ֹ�����ڹ��˵Ĺ�������©�����������²��ʽ��ͣ�������Ϊ�˳�ȥ����̿����Ȳ��������ʣ�����Ũ������ȴ�ᾧ��
��Ʒ���ȵļ��
��1��vmL0.010mol/L��ˮ��Һ��n��I2��=v��10-3L��0.010mol/L=v��10-5mol����
2Na2 S2O3����������I2
2 1
n��Na2 S2O3�� v��10-5mol
����n��Na2 S2O3��=2��v��10-5mol=2v��10-5mol
Na2 S2O3•5H2O���������Ϊ2v��10-5mol��248g/mol=496v��10-5g��
�����Ʒ����Ϊ$\frac{496v��10{\;}^{-5}g}{ag}$��100%=$\frac{0.496v}{a}$%��
�ʴ�Ϊ��$\frac{0.496v}{a}$%��
��������ʵ�������֪�����ɵ���Һ��ʹ FeCl3��Һ����Ѫ��ɫ��˵����SCN-���������ݵ���غ��Ԫ���غ��֪�����ӷ���ʽΪCN-+S2O32-=SCN-+SO32-��
�ʴ�Ϊ��CN-+S2O32-=SCN-+SO32-��
���� ����ͨ����ȡNa2S2O3•5H2O��ʵ������������������Ʊ���������ơ�����ʵ����������ʴ��ȵļ��㡢�ζ��������ȣ���Ŀ�Ѷ��еȣ���ȷʵ���������Ƽ�������ʵ������ǽ����Ĺؼ��������ֿ�����ѧ���ķ������������������Ӧ����ѧ֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
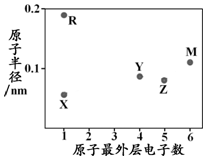
| A�� | �������Ӱ뾶��X��R | B�� | ��ۺ���������ԣ�Z��Y | ||
| C�� | M���⻯�ﳣ�³�ѹ��Ϊ���� | D�� | X��Y�����γ���������ṹ�ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ܢڢݢ� | B�� | �ܢ٢ڢݢ� | C�� | �ڢݢܢ٢� | D�� | �ܢݢڢ٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
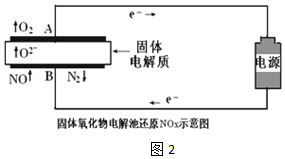
| ʵ����� | B������ | ��·��ͨ������ | �����ܵ��� | ����N2 |
| ʵ��1 | NO | 1mol | a KJ | 0.25mol |
| ʵ��2 | NO�Ϳ��� ��������NO2�� | 1mol | a KJ | 0.09mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
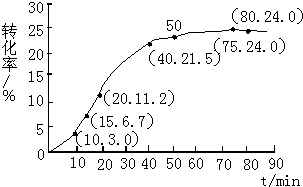 �������ˮ�ⷴӦ����ʽΪ��
�������ˮ�ⷴӦ����ʽΪ��| ��� | HCOOCH3 | H2O | HCOOH | CH3OH |
| ���ʵ���/mol | 1.00 | 1.99 | 0.01 | 0.52 |
| ��Ӧʱ�䷶Χ/min | 0��5 | 10��15 | 20��25 | 30��35 | 40��45 | 50��55 | 75��80 |
| ƽ����Ӧ����/��10-3mol•min-1�� | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
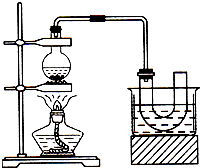 ʵ�����Ʊ������飨C2H5Br����װ�úͲ�����ͼ����֪������ķе�38.4�棩��
ʵ�����Ʊ������飨C2H5Br����װ�úͲ�����ͼ����֪������ķе�38.4�棩���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
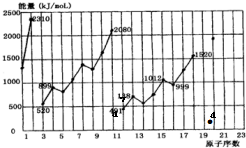 ��������������Ԫ�أ�����Ԫ�����ڱ��е�λ����ͼ��ʾ��
��������������Ԫ�أ�����Ԫ�����ڱ��е�λ����ͼ��ʾ��| �� | �� | ||
| �� | �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com