
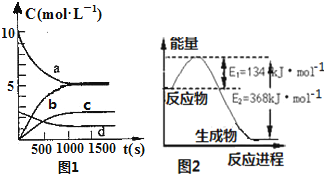
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
分析 (1)①化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值;温度低,化学平衡常数大,则正反应放热;
②NO2转化率为已转化的NO2物质的量与起始物质的量的百分比;增大NO2的转化率,促进反应的正向移动即可;
③N2O5为生成物且反应为可逆反应,反应不可能进行到底,以此判断表示N2O5的浓度的变化曲线;
(2)根据能量变化图,反应热等于=正反应的活化能减去逆反应的活化能,结合热化学方程式的书写规则书写;利用写出的热化学方程式,结合给出的热化学方程式,利用盖斯定律解答该题.
解答 解:(1)①化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,即K=$\frac{c{\;}^{2}(N{\;}_{2}O{\;}_{5})}{{c}^{4}(NO{\;}_{2})•c(O{\;}_{2})}$;温度低,化学平衡常数大,则正反应放热,
故答案为:$\frac{c{\;}^{2}(N{\;}_{2}O{\;}_{5})}{{c}^{4}(NO{\;}_{2})•c(O{\;}_{2})}$;放热;
②转化的NO2的物质的量为20mol-10.08mol=9.92mol,转化率为$\frac{9.92mol}{20mol}$=49.6%;
A、再充入NO2,转化的物质的量增大,但是起始的物质的量增大较多,转化率降低,故A错误;
B、加入气体比例与原平衡NO2的转化率相同,由于加入气体后,体系压强增大,NO2的转化率增大,故B正确;
C、该反应为放热反应,降低温度,化学平衡向右移动,故C正确;
D、反应气体浓度不变,化学平衡不移动,故D错误;
故选BC;
③N2O5为生成物浓度增大,反应为可逆反应,不可能进行到底,即N2O5的浓度不可能达到5mol/L,故选c;
(2)该反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol,所以热化学方程式为:①NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1;②2NO(g)+2CO(g)?N2(g)+2CO2(g),△H=-760.3kJ•mol-1,反应①×2-②,可得到:N2 (g)+2NO2 (g)?4NO(g)△H=+292.3kJ•mol-1,
故答案为:+292.3kJ•mol-1.
点评 本题考查化学平衡影响因素、化学平衡的计算,题目计算量较大,难度较大,关键是构建平衡建立的等效途径,中注意从正、逆不同方向建立的等效平衡转化率、反应热的关系.


科目:高中化学 来源: 题型:选择题
| A. | 2V正(B)=V逆(D) | |
| B. | 混合气体的密度保持不变 | |
| C. | 混合气体中B、C、D的浓度之比为2:2:1 | |
| D. | 混合气体的压强不随时间变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 mol A+2 mol B | |
| B. | 1 mol B+3 mol C+1 mol D | |
| C. | 3 mol C+2 mol D | |
| D. | 1 mol A+0.5 mol B+1.5 mol C+0.5 mol D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
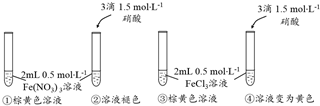
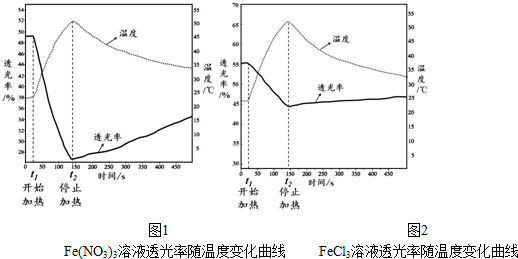
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
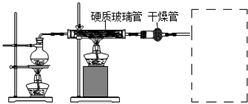
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
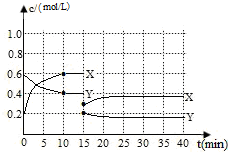 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物浓度随时间变化关系如下图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物浓度随时间变化关系如下图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) 物质的量(mol) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
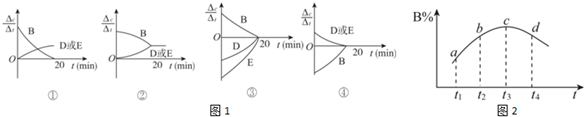
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
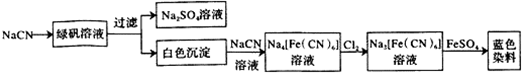
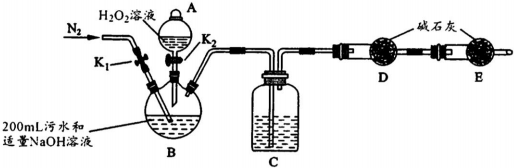
| 步骤1 | 关闭K1,打开K2,滴入足量H2O2溶液,对B加热.充分反应后,停止加热. |
| 步骤2 | 冷却后,用注射器穿过B装置的胶塞注入稀H2S04溶液. |
| 步骤3 | 打开K1,通入N2. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com