
| A. | Na2SO4 | B. | KNO3 | C. | Ca(NO3)2 | D. | KIO3 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b和c分别与a形成化合物的相对分子质量一定为b>c | |
| B. | a和d形成的化合物与水反应产生的气体可做燃料 | |
| C. | +6价的c和a、b形成离子化合物 | |
| D. | a、b、c和d四种元素组成的化合物的水溶液加入少量Na2CO3只产生气体,不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 20g重水中含有的电子数为10NA | |
| C. | 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.3NA | |
| D. | 1L 0.1mol/L NH4Cl溶液中含NH4+数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


 (R、R′可表示烃基或氢原子)
(R、R′可表示烃基或氢原子)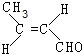 ,该分子中最多有9个原子共平面.
,该分子中最多有9个原子共平面. $→_{△}^{NaOH}$
$→_{△}^{NaOH}$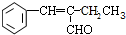 +H2O.
+H2O.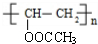 .
.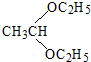 .合成路线流程图示例如下:
.合成路线流程图示例如下: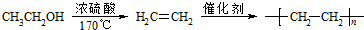
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
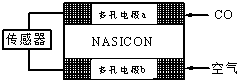
| A. | 负极的电极反应式为:CO+O2--2e-═CO2 | |
| B. | 工作时电极b作正极,O2-由电极a流向电极b | |
| C. | 工作时电子由电极a通过传感器流向电极b | |
| D. | 传感器中通过的电流越大,尾气中CO的含量越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若 A 为铁,D 为氢气,则 B 一定为酸 | |
| B. | 若 A、D 为化合物,B 为水,则 C 一定是气体单质 | |
| C. | 若 A、B、C、D 均为化合物,该反应一定属于复分解反应 | |
| D. | 若 A、B、C、D 均为 10 电子微粒,且 C 是可使湿润的红色石蕊试纸变蓝的气体,则 D 常温下一定呈液态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com