
���� N2��g��+3H2��g��?2NH3��g����H=-92.38kJ•mol-1������Ϊ1mol������3mol������ȫ��Ӧ����2mol����ʱ�ų�92.38kJ����������N2��g��+3H2��g��?2NH3��g�����ڿ��淴Ӧ�����淴Ӧ���ص��������淴Ӧ�����ܽ��е��ף����1 mol N2��g����3 mol H2��g��������ȫ��Ӧ����2 mol NH3��g��������ų���������С��92.38 kJ��
��� �⣺N2��g��+3H2��g��?2NH3��g����H=-92.38kJ•mol-1������Ϊ1mol������3mol������ȫ��Ӧ����2mol����ʱ�ų�92.38kJ����������N2��g��+3H2��g��?2NH3��g�����ڿ��淴Ӧ�����淴Ӧ���ص��������淴Ӧ�����ܽ��е��ף����1 mol N2��g����3 mol H2��g��������ȫ��Ӧ����2 mol NH3��g��������ų���������С��92.38 kJ���ʴ�Ϊ��С�ڣ��÷�Ӧ�ǿ��淴Ӧ�����ܱ������н��и÷�Ӧ���ﵽƽ��״̬��1molN2��g����3molH2��g��������ȫ��Ӧ����2molNH3��g��������ų���������С��92.38kJ��
���� ���⿼�����Ȼ�ѧ����ʽ������Ϳ��淴Ӧ���ص㣬�ѶȲ���ע����ȷ������淴Ӧ�Ȼ�ѧ����ʽ�����壮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʣ�࣬����Һ���ٵ�����������ֿ�ʼ�ܽ� | |
| B�� | ������ȫ���ܽ⣬����Һ��һ������Fe3+ | |
| C�� | ��������ʣ�࣬��Һ�п��ܺ���Fe2+ | |
| D�� | ������ȫ���ܽ⣬�Ҳ���336mL���壨��״���£�����b=0.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 60��36 | B�� | 36��60 | C�� | 2��1 | D�� | 1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | 30minʱ��С�ݻ� | |
| B�� | 40minʱ������� | |
| C�� | 0��20min��A��ƽ����Ӧ����Ϊ0.05mol•L-1•min-1 | |
| D�� | ����ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1.0��1{0}^{-14}}{2.4��1{0}^{-7}}$mol•L-1 | B�� | 0.1��10-7 mol•L-1 | ||
| C�� | 2.4��10-7 mol•L-1 | D�� | c��OH-����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

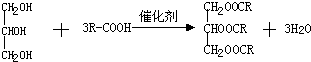 ��
��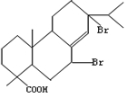 ��
��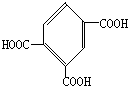 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
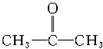 �Ĺ�����Ϊ
�Ĺ�����Ϊ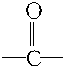 ������ͪ�����ʣ����������ʵķ���ʽΪC3H6O�����ǵĹ�ϵ��ͬ���칹�壮
������ͪ�����ʣ����������ʵķ���ʽΪC3H6O�����ǵĹ�ϵ��ͬ���칹�壮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com