
ijѧ��Ϊ�ⶨδ֪Ũ�ȵ�������Һ����֪�ζ�ʱ��ѡ���ָʾ����ʯ���̪��,ʵ�����£���1.00m L������������100mLϡH2SO4��Һ����0.14mol•L��1��NaOH��Һ�ζ�����ϡH2SO4 25.00mL���ζ���ֹʱ����NaOH��Һ15.00mL��
L������������100mLϡH2SO4��Һ����0.14mol•L��1��NaOH��Һ�ζ�����ϡH2SO4 25.00mL���ζ���ֹʱ����NaOH��Һ15.00mL��
��1����ѧ���ñ�0.14mol•L��1NaOH��Һ�ζ������ʵ��������£�
A������ʽ�ζ���ȡϡH2SO4 25.00mL��ע����ƿ�У�����ָʾ����
B���ô��ⶨ����Һ��ϴ��ʽ�ζ���
C��������ˮϴ�ɾ��ζ���
D��ȡ�¼�ʽ�ζ����ñ���NaOH��Һ��ϴ����Һע���ʽ�ζ��̶ܿȡ�0������2~3cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ�����̶ȡ�0����0���̶�����
E�����ζ����Ƿ�©ˮ
F����ȡ��ƿ�����ظ�����һ��
G������ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶�
�ٵζ���������ȷ˳���� ��
�ڸõζ�������Ӧѡ�õ�ָʾ���� ��
����G�� �������ȷ���յ㣿 ��
�������ȷ���յ㣿 ��
��2����ʽ�ζ���������ˮ��ϴ��δ�ô���Һ��ϴ���µζ�������ƫС������ƫ��ǡ�ú��ʡ��� ��
��3������ȷŨ�ȵ�ϡH2SO4��Һ������ʹ�õ���Ҫ������ ��
��4���ñ�NaOH��Һ�ζ�ʱ��Ӧ����NaOH��Һע�� ����ס����ҡ����С�
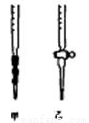
��5���۲��ʽ�ζ��ܶ���ʱ�����ζ�ǰ���ӣ��ζ����ӣ������ᵼ�²�õ�ϡH2SO4��ҺŨ�Ȳⶨֵ ��ѡ�ƫ��ƫС������Ӱ�족����
��6������������ᣨϡ��ǰ�����ᣩ��Һ�����ʵ���Ũ�� ������ �����С������λ����
 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ�����гǽ����ص��������һ�����л�ѧ���������棩 ���ͣ�ѡ����
���й��ڽ������������ȷ����
A�������˶����ǽ��������е��˶���ʽ��
B������������ʱ�����������ЧӦ������Ϊ���ӶԹ��ɢ����ɵ�
C����������������ֽ�����Բ����ù��˵ķ������뽺�����Һ
D�������ܷ�����Ӿ�����Խ������ɣ����ڳ��ֵ����ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA���������ӵ�������ֵ��������Ȼ�ѧ����ʽC2H2��g��+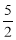 O2(g) ��2CO2(g)+H2O(l) ��H=��1300 kJ��mol��1��˵���У���ȷ����( )
O2(g) ��2CO2(g)+H2O(l) ��H=��1300 kJ��mol��1��˵���У���ȷ����( )
A����10NA������ת��ʱ���÷�Ӧ����1300 kJ������
B����1NA��ˮ����������ΪҺ��ʱ������1300 kJ������
C����2NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
D����8NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�˲��и�һ�����л�ѧ���������棩 ���ͣ�ѡ����
���ʵ���Ũ����ͬ������ء�����ء�����أ�K3PO4��������Һ�У���ʹ�����ӵ����ʵ�����ͬ������������Һ�������Ϊ�� ��
A��3��2��1 B��6��3��2 C��2�� 3��6 D��1��2��3
3��6 D��1��2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�˲��и�һ�����л�ѧ���������棩 ���ͣ�ѡ����
�����Ȼ�̼��ȡ��ı���ˮ��Һ�еĵ⣬����˵������ȷ���ǣ� ��
A��ʵ��ʹ�õ���Ҫ�����Ƿ�Һ©��
B����Һʱ��ˮ�ӷ�Һ©���¿�������������Ȼ�̼��Һ��©���Ͽڵ���
C���������Ȼ�̼�е��ܽ�ȱ���ˮ�е��ܽ�ȴ�
D��������Ȼ�̼��Һ���Ϻ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�˲��и߶������л�ѧ���������棩 ���ͣ�ѡ����
��������0. 1mol/L������Һ�У���˵��CH3COOH����ﵽƽ����� �� ��
1mol/L������Һ�У���˵��CH3COOH����ﵽƽ����� �� ��
A����Һ�Ե����� B����Һ��CH3COOH���ٵ���
C����Һ��������Ũ�Ȳ��ٸı� D��c(H+)��c(CH3COO��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�˲��и߶������л�ѧ���������棩 ���ͣ�ѡ����
���ܱ������з������з�ӦaA��g��?cC��g��+dD��g����ѹ���ݻ���ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ���ǣ� ��
A��A��ת���ʱ�� B��ƽ��������Ӧ�����ƶ�
C��D������������ D��a��c+d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�����и�һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����״���µ�a LHCl��������l000gˮ�У��õ��������ܶ�Ϊbg/cm3�������������ʵ���Ũ���ǣ� ��
A.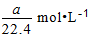 B.
B.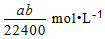
C.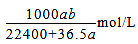 D.
D.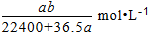
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ����12���¿���ѧ�Ծ��������棩 ���ͣ������
�о���������ķ�Ӧ���������������Ի�������Ⱦ����Ҫ���塣�����¶Ⱦ�������Ļ�ѧ��Ӧ����������2NO(g)+O2(g) 2NO2(g)������ȴ�����¶ȵ����߶���С��ij��ѧС��Ϊ�о������������ʵ��ԭ��������֪2NO(g)+O2(g)
2NO2(g)������ȴ�����¶ȵ����߶���С��ij��ѧС��Ϊ�о������������ʵ��ԭ��������֪2NO(g)+O2(g) 2NO2(g)�ķ�Ӧ���̷�������
2NO2(g)�ķ�Ӧ���̷�������
��2NO(g) N2O2(g)(��)��v1��=k1��c2(NO)��v1��=k1��c(N2O2)∆H1<0
N2O2(g)(��)��v1��=k1��c2(NO)��v1��=k1��c(N2O2)∆H1<0
��N2O2(g)+O2(g) 2NO2(g)(��)��v2��=k2��c(N2O2)c(O2)��v2��=k2��c2(NO2)∆H2
2NO2(g)(��)��v2��=k2��c(N2O2)c(O2)��v2��=k2��c2(NO2)∆H2 <0
<0
��ش��������⣺
��1����Ӧ2NO(g)+O2(g) 2NO2(g)��∆H= (�ú�∆H1��∆H2��ʽ�ӱ�ʾ)��һ���¶��£���Ӧ2NO(g)+O2(g)
2NO2(g)��∆H= (�ú�∆H1��∆H2��ʽ�ӱ�ʾ)��һ���¶��£���Ӧ2NO(g)+O2(g) 2NO2(g)�ﵽƽ��״̬����д����k1����k1�桢k2����k2���ʾ��ƽ�ⳣ������ʽK= �������¶ȣ�Kֵ (���������С�����䡱)��
2NO2(g)�ﵽƽ��״̬����д����k1����k1�桢k2����k2���ʾ��ƽ�ⳣ������ʽK= �������¶ȣ�Kֵ (���������С�����䡱)��
��2������2NO(g)+O2(g) 2NO2(g)���ʵ��Ƿ�Ӧ�ڣ���Ӧ�ٵĻ��E1�뷴Ӧ�ڵĻ��E2�Ĵ�С��ϵΪE1 E2(�>������<����=��)���������ʷ��̷����������¶ȸ÷�Ӧ���ʼ�С��ԭ���� ��
2NO2(g)���ʵ��Ƿ�Ӧ�ڣ���Ӧ�ٵĻ��E1�뷴Ӧ�ڵĻ��E2�Ĵ�С��ϵΪE1 E2(�>������<����=��)���������ʷ��̷����������¶ȸ÷�Ӧ���ʼ�С��ԭ���� ��
A��k2������c(N2O2)����
B��k2����С��c(N2O2)��С
C��k2������c(N2O2)��С
D��k2������c(N2O2)����
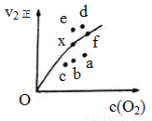
��ʵ�����ݵõ�v2��~[O2]�Ĺ�ϵ������ͼ��ʾ����x�����ߵ�ijһ�¶�ʱ����Ӧ���´ﵽƽ�⣬���Ϊ��Ӧ�ĵ�Ϊ (����ĸ)��
��3����ҵ�Ͽ��ð�ˮ��ΪNO2�����ռ���NO2ͨ�백ˮ�����ķ�Ӧ��2NO2+2NH3��H2O=NH4NO3+NH4NO2+H2O������Ӧ�����Һ������ȳʺ�ɫ����Ӧ����Һ��c(NH4+) c(NO3-)+c(NO2-)(�>����<����=��)����ҵ��Ҳ���õ�ⷨ���������������Ⱦ��������ͼ��ʾ�������缫�����������������մɣ���һ�������¿ɴ���O2-��
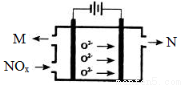
�õ��������ĵ缫��Ӧʽ�� ����������������N�Ļ�ѧʽ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com