
【题目】化合物丙由如下反应制得:C4H10O ![]() C4H8
C4H8 ![]() C4H8Br2(丙),丙的结构简式不可能是( )
C4H8Br2(丙),丙的结构简式不可能是( )
A.CH3CH2CHBrCH2Br
B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3
D.(CH3)2CBrCH2Br
【答案】B
【解析】解:甲能在浓硫酸作用下发生消去反应生成C4H8 , 说明甲中含有羟基,甲为醇,乙为烯烃,丙为卤代烃,其中甲的结构可能有4种:CH3CH2CHOHCH3、CH3COH(CH3)2、CH3CH2CH2CH2OH、(CH3)2CHCH2OH,乙的结构有3种:CH3﹣CH2﹣CH=CH2、CH3﹣CH=CH﹣CH3、 ![]() ,乙→丙的反应为
,乙→丙的反应为 ![]() 与Br2的加成反应,则丙中应含有则分子中应含有﹣CHBr﹣CHBr﹣结构,则丙的结构不可能为CH3CH(CH2Br)2 , 故选B. 甲能在浓硫酸作用下发生消去反应生成C4H8 , 说明甲中含有羟基,乙应为烯烃,即丁烯,丁烯与溴发生加成反应生成二溴丁烷,则分子中应含有﹣CHBr﹣CHBr﹣结构,以此解答该题.
与Br2的加成反应,则丙中应含有则分子中应含有﹣CHBr﹣CHBr﹣结构,则丙的结构不可能为CH3CH(CH2Br)2 , 故选B. 甲能在浓硫酸作用下发生消去反应生成C4H8 , 说明甲中含有羟基,乙应为烯烃,即丁烯,丁烯与溴发生加成反应生成二溴丁烷,则分子中应含有﹣CHBr﹣CHBr﹣结构,以此解答该题.


科目:高中化学 来源: 题型:
【题目】利用下图装置(夹持装置略)制取和收集纯净、干燥的氨气,并探究 氨气的性质。

(1)关闭装置I中的止水夹,向分液漏斗中加入适量水,打开活塞,说明装置I 气密性良好的现象是____________________________________________________。
(2)利用装置I制取氨气,应选用的试剂为浓氨水_______ 和 ______(填序号)。
A.氢氯化钠 B.浓硫酸 C.硝酸钾 D.生石灰
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接_____, 接 , 接 。
(4)将氨气通入盛有氧化铜粉末的玻璃管中,加热有红色固体和无色气体单质生成,证明氨气具有_____________性,反应的化学方程式是__________________________________。
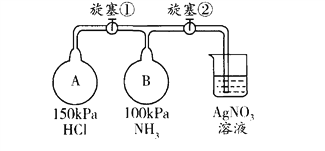
(5)收集氨气,按下图玻璃装置进行实验。先打开旋塞①,B瓶中产生白色的烟,原因是______________________ (用化学方程式表示);稳定后,关闭旋塞①,再打幵旋塞②,B瓶中的现象是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性实验小组欲验证浓硝酸在与Cu、Ag 合金的反应过程中除生成NO2气体外,还会有少量NO生成。查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。”为此,他们设计了如下图所示的装器。

请回答下列问题
(1)写出A中银与HNO3反应时所有可能的离子方程式_____________________。
(2)实验开始时,打开分液漏斗前要先打开活塞______( 填“K1”或“K2”),其目的是___________。
(3)装置中B瓶选用的试剂______________。
a.H2O b.浓硫酸 c.NaOH 熔液
(4)装置E中长颈漏斗的作用____________。
(5)反应停止后,欲想证明有NO生成,需要怎样操作:__________,当出现何种现象说明有NO生成____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室研究Fe与H2SO4的反应

【实验分析】
(1)实验I中,铁与稀硫酸反应的离子方程式为________________。
(2)实验Ⅱ中,铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止,这一现象被称为___________________。
(3)实验Ⅲ,己知: 浓H2SO4 的沸点为338.2℃,加热试管A,温度保持在250℃~300℃,产生大量气体B中品红褪色,D处始终未检测到可燃性气体。A 中产生的气体是__,装置C 的作用是________________。
(4)实验Ⅲ结束后,经检验A 中既有Fe3+又有不少的Fe2+。
①若要检验Fe3+和Fe2+,下列试剂组可行的是______ (填字母)。
A.KSCN、Fe粉 B.KSCN、酸性KMnO4溶液 C.KSCN、氯水
[实验反思]
(5)①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于_____,稀硫酸的氧化性源于_______________。
②影响反应产物多样性的因素有_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
A. 实验室制乙烯
实验室制乙烯
B.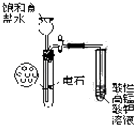 实验室制乙炔并验证乙炔发生氧化反应
实验室制乙炔并验证乙炔发生氧化反应
C.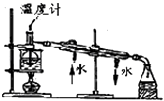 实验室中分馏石油
实验室中分馏石油
D.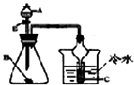 若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的强弱(不考虑醋酸的挥发)
若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的强弱(不考虑醋酸的挥发)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制500 mL 0.2 mol/L的Na2SO4溶液,实验操作步骤有:
A.在天平上称出14.2 g硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却至室温。
B.把制得的溶液小心地转移到容量瓶中。
C.继续向容量瓶中加蒸馏水至液面距刻度线1-2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2-3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶瓶塞塞紧,充分摇匀.请填写下列空白:
(1)操作步骤的正确顺序为(填序号)_________。
(2)本实验用到的基本仪器已有烧杯、天平托盘(带砝码、镊子)、玻璃棒,还缺少的仪器是_____、____、____。
(3)下列情况会使所配溶液浓度偏高的是(填序号)________。
a.某同学观察液面的情况如右图所示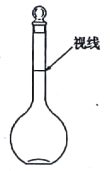
b.没进行上述的操作步骤D
c.加蒸馏水时,不慎超过了刻度线
d.砝码上沾有杂质
e.容量瓶使用前内壁沾有水珠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com