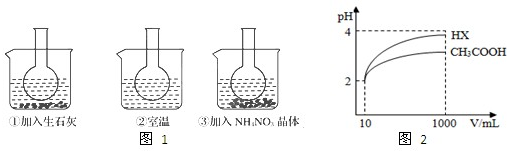
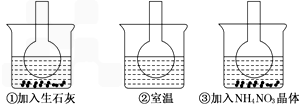
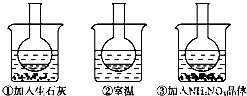
如图1所示三个烧瓶中分别装入含酚酞的0.01mol?L
-1 CH
3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH
4NO
3晶体,烧杯②中不加任何物质.
(1)含酚酞的0.01mol?L
-1 CH
3COONa溶液显浅红色的原因为:______(用离子方程式表示).
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是______.
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH
4NO
3溶于水时放出热量 D.NH
4NO
3溶于水时吸收热量
(3)向0.01mol?L
-1 CH
3COONa溶液中加入少量浓盐酸,则CH
3COO
-水解平衡移动的方向为________; 加入NaOH固体,则CH
3COO
-水解平衡移动的方向为______(填“左”、“右”或“不移动”)
(4)25℃时,CH
3COOH与CH
3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH
3COO
- )-c(Na
+)=______.(填准确数值)
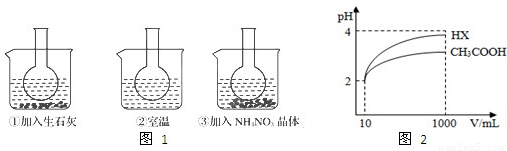
(5)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图2,则HX的酸性______(填“>”、“=”或“<”)醋酸的酸性;稀释后,HX溶液中水电离出来的c(H
+)______醋酸溶液水电离出来c(H
+)(填“>”、“=”或“<”).