
用已被部分氧化的金属屑A制备某工业常用盐C的步骤如下:
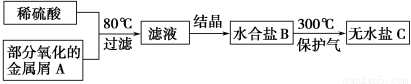
将C溶于水,向其中滴入NaOH溶液,出现白色沉淀,后逐渐变为红褐色,下列判断正确的是
A.过滤所得的残渣中一定没有金属A
B.滤液可能是CuSO4溶液或MgSO4溶液
C.水合盐B可能是FeSO4·7H2O
D.无水盐C可能是Fe2(SO4)3
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省福州市高一上学期期中化学试卷(解析版) 题型:填空题
有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、KOH中的一种或几种,为证明其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是 ,原混合物中一定不含有 ;
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原混合物中一定含有 。 该反应的离子方程式为 ;
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验(2)中产生的气体里含有 。
(4)向实验(3)中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有 ,根据实验全过程推断,原混合物中还含有 。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省福州市高一上学期期中化学试卷(解析版) 题型:选择题
下列化学反应中,不属于氧化还原反应的是
A.KClO+CO2+H2O === KHCO3+HClO B.H2+CuO  Cu + H2O
Cu + H2O
C.Fe2O3 +3CO 2 Fe + 3CO2 D.2CO + O2
2 Fe + 3CO2 D.2CO + O2  2CO2
2CO2
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省福州市高一上学期期中化学试卷(解析版) 题型:选择题
近来我国某些城市将市区汽车排气管装上催化转换器,目的是:使碳氢化合物迅速转化为二氧化碳和水;氮的氧化物转化为氮气,使汽车尾气得到净化。关于这两个目的所涉及的物质变化,下列说法正确的是
A.均为氧化反应 B.均为化学变化
C.均为物理变化 D.前者为化学变化,后者为物理变化
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(理)试卷(解析版) 题型:填空题
(18分)下表为长式周期表的一部分,其中的编号代表对应的元素。

试填空。
(1)写出元素D与A形成的化合物的电子式 ,该化合物分子的空间构型是 ,其中元素D的杂化方式为 。
(2)J的离子结构示意图 ;K元素在周期表的位置 。元素L基态原子的电子排布式 。
(3)E、H、I 这三种元素的第一电离能由大到小的顺序是(填对应的元素符号) ;
(4)由D、J的氢化物相互作用所生成的物质所含化学键有下列的 。
A、离子键
B、非极性键
C、极性键
D、金属键
E、配位键
(5)用氢键表示式写出F的氢化物水溶液中所有氢键
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期中化学(理)试卷(解析版) 题型:选择题
有关晶体的下列说法中不正确的是
A.分子晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,则晶体的熔点越高
C.冰融化时水分子中H—O键未发生断裂
D.冰的密度比液态水的密度小与水分子间的氢键有关
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期末考试化学试卷(解析版) 题型:填空题
铁是目前用途最广,用量最大的金属。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是 。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: 。
(3)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
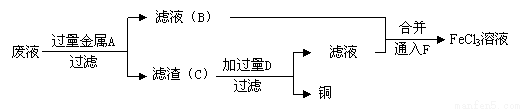
①滤渣C的化学式为 ;
②试剂F宜选用______(填选项序号),通入F的目的是_______________;
A.酸性KMnO4溶液 B.氯水 C.溴水
(4)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是 ;②溶液组成的测定:取30.0mL待测溶液,加入足量的AgNO3溶液,得25.83g白色沉淀。则溶液中c(Cl-)= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列操作中,能使电离平衡H2O H++OH-向右移动且溶液呈酸性的是
H++OH-向右移动且溶液呈酸性的是
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com