
����Ŀ�����������һ�����͵�أ�����Ҫ�ص��ǿ���ͨ���������Һ��ѭ���������ڵ���ⲿ���ڵ������Һ���Ա��ֵ���ڲ��缫��Χ��ҺŨ�ȵ��ȶ����ҹ�ij�о�С���¿�����һ�����������ͼ��ʾ������˵������ȷ���ǣ�������

A.������b������������������a��
B.�õ�ع���ʱ��H+����a���õ���
C.b���ĵ缫��ӦΪCu-2e-�TCu2+
D.�õ�ع���һ��ʱ�����Ҫ����H2SO4
���𰸡�B
��������
����ͼʾ�����Ǧ���ص�ԭ�����õ���ܷ�ӦΪCu+PbO2+2H2SO4�TCuSO4+PbSO4+2H2O����ͭʧ���ӷ���������ӦΪ�������缫��ӦʽΪ��Cu-2e-�TCu2+��PbO2�õ��ӷ�����ԭ��ӦΪ��������ӦʽΪ��PbO2+4H++SO42-+2e-�TPbSO4+2H2O���ݴ˷������
A������ͼʾ������ܷ�ӦΪCu+PbO2+2H2SO4�TCuSO4+PbSO4+2H2O��ͭʧ���ӷ���������ӦΪ������PbO2�õ��ӷ�����ԭ��ӦΪ����������bΪ������aΪ������ԭ����е����ɸ���������������������A��ȷ��
B��PbO2�õ��ӷ�����ԭ��ӦΪ�������缫��ӦʽΪ��PbO2+4H++SO42-+2e-�TPbSO4+2H2O�����Ըõ�ع���ʱ��H+����a������û�еõ����ӣ���B����
C����������������ͭʧ���ӷ���������ӦΪ������b���ĵ缫��ӦʽΪ��Cu-2e-�TCu2+����C��ȷ��
D���ɵ���ܷ�ӦΪCu+PbO2+2H2SO4�TCuSO4+PbSO4+2H2O����õ�ع���һ��ʱ�����Ҫ����H2SO4����D��ȷ��
��ѡB��


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ɳ������KOH��ҺΪ���Һ���ŵ�ʱ���ܷ�ӦΪFe��Ni2O3��3H2O=Fe(OH)2��2Ni(OH)2�������йظõ�ص�˵����ȷ����
A.�ŵ�ʱ��������ӦʽΪFe-2e-��2OH-=Fe(OH)2
B.�ŵ�ʱ��K+��Fe�缫Ǩ��
C.���ʱ��������ӦʽΪ2Ni(OH)2-2e-��2OH-=Ni2O3��3H2O
D.���ʱ������������Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ظ���س������л��ϳɵ��������ʹ����ȡ��ɺ�����Һ����Ҫ��Cr3+��Fe3+��K+��SO42-�ȣ��Ʊ�K2Cr2O7����������ͼ��ʾ��
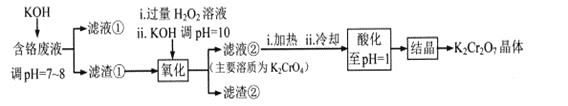
��֪��I �����������£�H2O2�ܽ�Cr2O72-��ԭΪCr3+
II��ؽ��������γ��������������pH��Χ���£�

�ش��������⣺
��1�������ڵ���Ҫ�ɷ�Ϊ___________���ѧʽ����
��2��д���������������з�Ӧ�Ļ�ѧ����ʽ_______________��
��3����������������Ŀ����__________________��
��4�����ữ�������з�����Ӧ2CrO42-+2H+![]() Cr2O72-+H2O ��K=4��1014 L3.mol3����֪�����ữ������Һ��c��Cr2O72-��=1.6��10-3mol/L����Һ��c��CrO42-��=_________
Cr2O72-+H2O ��K=4��1014 L3.mol3����֪�����ữ������Һ��c��Cr2O72-��=1.6��10-3mol/L����Һ��c��CrO42-��=_________
��5�����ᾧ����õ�K2Cr2O7��M=294g.mol-1����Ʒ0.5000 g�������ܽ����ϡH2SO4�ữ������Ũ��Ϊ1.0000 mol.L-1 ��NH4��2Fe��SO4��2����Һ�ζ����ζ��յ����ı���Һ�����Ϊ 9.00 mL�����Ʒ�Ĵ���Ϊ_____________��[�ζ���ӦΪ��K2Cr2O7+6��NH4��2Fe��SO4��2+7H2SO4 =K2SO4 +Cr2��SO4��3 +6��NH4��2SO4+3Fe2��SO4��3+7H2O]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����![]()
![]()
A.����ʽΪ![]() ���л���ṹ����2������ͬ���칹����4��
���л���ṹ����2������ͬ���칹����4��
B.��ͼ�ɱ�ʾΪ���Ȼ�̼�����ģ��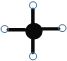
C.���ȼ���ֻ��һ�ֽṹ��������ͬ���칹�壬֤����������������ṹ
D.����ķ���ʽ�ɱ�ʾΪ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ2L���ܱ������У�3molX��3molY������Ӧ��3X(g)��Y(g)![]() 2Z(g) ��H>0����60s�ﵽƽ�⣬����0.4molZ������˵����ȷ���ǣ� ��
2Z(g) ��H>0����60s�ﵽƽ�⣬����0.4molZ������˵����ȷ���ǣ� ��
A.60s��ƽ����Ӧ����v(X)��0.05mol/(L��s)
B.�����������䣬�����¶ȣ�����Ӧ���������淴Ӧ���ʼ�С
C.�����������䣬����ʼͶ��2molX��2molY��������Y��ת���ʼ�С
D.�����������䣬�����������Ϊ4L��Z��ƽ��Ũ�ȱ�Ϊԭ����һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. 0.1mol/LC6H5ONa��Һ����c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
B. Na2CO3��Һ��ˮϡ�ͺָ���ԭ�¶ȣ�pH��Kw����С
C. ��Na2S��Һ�м���AgC1���壬��Һ��c(S2-)�½�
D. pH=5��CH3COOH��Һ��pH=5��NH4Cl��Һ�У�c(H+)�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ�ĺ;����˹��Ʊ��ľ��嶼���ڸ���ȱ�ݣ����磬ij��NiO�����оʹ�����ͼ��ʾ��ȱ�ݣ�һ��Ni2+��ȱ����������Ni2+������Ni3+��ȡ������������Գʵ����ԣ�����������Ni��O�ı�ֵȴ�����˱仯��ij��������Ʒ���ΪNi0.97O����þ�����Ni3+��Ni2+��������֮��Ϊ( )
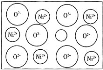
A.6��85B.6��91C.5��91D.5��85
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2H4��һ�ָ�Ч���Ļ��ȼ�ϡ�8gN2H4(g)��ȫȼ�����ɵ�������̬ˮʱ���ų�133.5kJ�������������Ȼ�ѧ����ʽ����ȷ���ǣ� ��
A.![]() N2H4(g)��
N2H4(g)��![]() O2(g)=
O2(g)=![]() N2(g)��H2O(g) ��H����267kJ��mol��1
N2(g)��H2O(g) ��H����267kJ��mol��1
B.N2H4(g)��O2(g)=N2(g)��2H2O(g) ��H����534kJ��mol��1
C.N2H4(g)��O2(g)=N2(g)��2H2O(g) ��H����534kJ��mol��1
D.N2H4(g)��O2(g)=N2(g)��2H2O(l) ��H����133.5kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к��зḻ��þ��Դ��ijͬѧ����˴�ģ�⺣ˮ���Ʊ�MgO��ʵ�鷽����

ģ�⺣ˮ�е�����Ũ��/mol��L��1 | Na�� | Mg2�� | Ca2�� | Cl�� | HCO3�� |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
ע����Һ��ij�����ӵ�Ũ��С��1.0��10��5 mol��L��1������Ϊ�����Ӳ����ڣ�ʵ������У�������Һ������䡣Ksp[CaCO3]��4.96��10��9��Ksp[MgCO3]��6.82��10��6��Ksp[Ca(OH)2]��4.68��10��6��Ksp[Mg(OH)2]��5.61��10��12������˵����ȷ���ǣ� ��
A.������XΪCaCO3
B.��ҺM�д���Mg2����������Ca2��
C.��ҺN�д���Mg2����Ca2��
D.�����������Ϊ����4.2 g NaOH���壬������YΪCa(OH)2��Mg(OH)2�Ļ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com