
 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.某学生在实验室利用如图的实验装置制备乙酸乙酯并研究其反应条件.
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.某学生在实验室利用如图的实验装置制备乙酸乙酯并研究其反应条件.| 物质 | 沸点/°C | 密度/g?cm-3 |
| 乙醇 | 78.0 | 0.79 |
| 乙酸 | 117.9 | 1.05 |
| 乙酸乙酯 | 77.5 | 0.90 |
| 异戊醇 | 131 | 0.8123 |
| 乙酸异戊酯 | 142 | 0.8670 |
| 实验编号 | 试管Ⅰ中的试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
分析 (1)乙酸、乙醇在浓硫酸做催化剂条件下发生反应生成乙酸乙酯,浓硫酸稀释产生的量的热,密度大于水,为防止酸液飞溅,应先加入乙醇,然后在加入浓硫酸和乙酸;加热浓硫酸、乙醇、乙酸混合液体容易发生爆沸;浓硫酸密度大,稀释产生大量的热,混合时应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸,据此判断加入顺序;可逆反应中,增大一种反应物的浓度可以提高另一种反应物的转化率;
(2)化学平衡常数为生成物浓度幂之积与反应物浓度幂之积之比;
(3)乙醇、乙酸易挥发,制备的乙酸乙酯中含有乙醇和乙酸,乙醇易溶于水,乙酸能够与碳酸钠溶液反应,乙酸乙酯在饱和碳酸钠溶液中溶解度不大,所以可以用饱和碳酸钠溶液除去乙醇、乙酸,降低乙酸乙酯的溶解度;分离两种互不相溶的液体应选择分液操作,用到的主要仪器为:分液漏斗;
(4)①通过对照实验,证明H+对酯化反应具有催化作用,应保证氢离子浓度相等与物质的量相等;
②对比浓硫酸、稀硫酸生成乙酸乙酯的量的多少,说明浓硫酸浓硫酸的吸水性能够提高乙酸乙酯产率,根据平衡移动原理分析;
③乙酸、乙醇易挥发,也可能发生其它副反应;
(5)依据乙酸异戊酯沸点结合化学平衡移动影响因素解答;
解答 解:(1)乙酸、乙醇在浓硫酸做催化剂条件下发生反应生成乙酸乙酯,浓硫酸稀释产生的量的热,密度大于水,为防止酸液飞溅,应先加入乙醇,然后在加入浓硫酸和乙酸,所以试管1中添加顺序是先加入乙醇,再加入浓硫酸,最后加入乙酸,加热浓硫酸、乙醇、乙酸混合液体容易发生爆沸,为防止发生爆沸应加入:碎瓷片;浓硫酸密度大,应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸;添加顺序依次3mL乙醇、2mL浓H2SO4、2mL乙酸;可逆反应中,增大一种反应物的浓度可以提高另一种反应物的转化率,所以乙醇过量的目的是:提高乙酸的转化率;
故答案为:乙醇、浓硫酸、乙酸、碎瓷片;3mL乙醇、2mL浓H2SO4、2mL乙酸;提高乙酸的转化率;
(2)依据方程式:CH3COOH(g)+CH3CH2OH(g)$?_{△}^{浓硫酸}$CH3COOCH2CH3(g)+H2O(g),可知反应的平衡常数K=$\frac{[C{H}_{3}COOC{H}_{2}C{H}_{3}][{H}_{2}O]}{[CH{\;}_{3}COOH][C{H}_{{\;}_{3}}C{H}_{2}OH]}$;
故答案为:$\frac{[C{H}_{3}COOC{H}_{2}C{H}_{3}][{H}_{2}O]}{[CH{\;}_{3}COOH][C{H}_{{\;}_{3}}C{H}_{2}OH]}$;
(3)乙醇、乙酸易挥发,制备的乙酸乙酯中含有乙醇和乙酸,乙醇易溶于水,乙酸能够与碳酸钠溶液反应,方程式:2CH3COOH+Na2CO3═2CH3COONa+CO2↑+H2O,乙酸乙酯在饱和碳酸钠溶液中溶解度不大,所以可以用饱和碳酸钠溶液除去乙醇、乙酸,降低乙酸乙酯的溶解度;分离两种互不相溶的液体应选择分液操作,用到的主要仪器为:分液漏斗;
故答案为:饱和碳酸钠溶液;2CH3COOH+Na2CO3═2CH3COONa+CO2↑+H2O;分液漏斗;
(4)①通过对照实验,证明H+对酯化反应具有催化作用,应保证氢离子浓度相等与物质的量相等,故HCl的浓度为3mol/L×2=6mol/L,盐酸体积为6mL,
故答案为:6;6;
②催化剂为浓硫酸生成有机层厚度比3mol•L-1 H2SO4时生成有机层厚度厚,说明浓硫酸浓硫酸的吸水性能够提高乙酸乙酯产率,原因是:浓硫酸可以吸收酯化反应中生成的水,降低了生成物浓度使平衡向生成乙酸乙酯的方向移动,
故答案为:AC;浓硫酸可以吸收酯化反应中生成的水,降低了生成物浓度使平衡向生成乙酸乙酯的方向移动;
③乙酸、乙醇易挥发,温度过高大量乙酸、乙醇未经反应就脱离反应体系,且温度过高发生其他反应,导致产率降低,故答案为:大量乙酸、乙醇未经反应就脱离反应体系;温度过高发生其他反应;
(5)乙酸异戊酯沸点142度,加热难以蒸发,所以主要在试管中得到,产物不能分离,生成物浓度增大,平衡逆向移动,抑制反应进行,所以产率会低;
故答案为:试管;低;
点评 本题考查有机物制备实验、探究实验,(4)中注意利用控制变量法分析,综合考查学生实验能力、分析能力与知识迁移运用能力,难度中等,注意化学平衡移动影响因素.


科目:高中化学 来源:2016-2017学年安徽师大附中高二上10月月考化学卷(解析版) 题型:选择题
已知:C(s)+H2O(g)===CO (g) +H2 (g) ΔH=a kJ·mol-1
2C(s)+ O2(g)===2CO (g) ΔH= - 220 kJ·mol-1
H-H、O==O和O- H键的键能分别为436、496和462 kJ·mol-1,则 a 为
H键的键能分别为436、496和462 kJ·mol-1,则 a 为
A.-332 B.+130 C.+350 D.-118
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点(℃) | 56.2 | 77.06 | 78 | 117.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.
如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
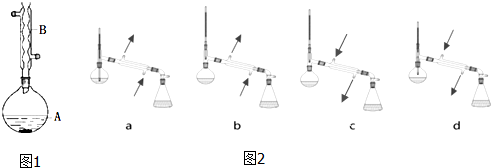
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 化学反应吸收或放出热量的多少与参加反应的物质的多少无关 | |
| D. | C(石墨,s)═C(金刚石,s)△H>0,所以石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
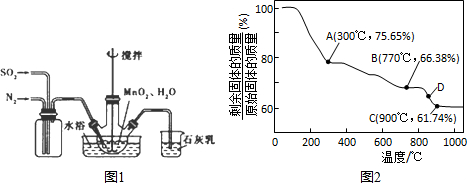
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com