
| A. | 2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O | |
| B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| C. | Mg+2HCl=MgCl2+H2↑ | |
| D. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
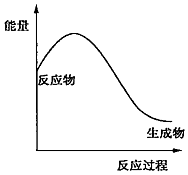
分析 由图可知,反应物总能量大于生成物总能量,为放热反应,结合铝热反应、金属与水或酸的反应、燃烧反应、中和反应为放热反应来解答.
解答 解:A.2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O为吸热反应,与图象不符,故A选;
B.2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3为放热反应,与图象相符,故B不选;
C.Mg+2HCl=MgCl2+H2↑为放热反应,与图象相符,故C不选;
D.C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2为放热反应,与图象相符,故D不选;
故选A.
点评 本题考查反应热与焓变,为高频考点,把握图中能量变化、反应中能量变化为解答的关键,侧重分析与应用能力的考查,注意归纳常见的放热反应,题目难度不大.


科目:高中化学 来源: 题型:多选题

| A. | X难溶于乙醇 | |
| B. | 酒中的少量丁酸能抑制X的水解 | |
| C. | X完全燃烧后生成CO2和H2O的物质的量比为1:1 | |
| D. | 分子式为 C5H10O2且能与NaHCO3溶液反应生成气体的物质有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
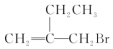
| A. | 该物质可以发生水解反应 | |
| B. | 该物质能和AgNO3溶液反应产生AgBr沉淀 | |
| C. | 该物质可以发生消去反应 | |
| D. | 该物质不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

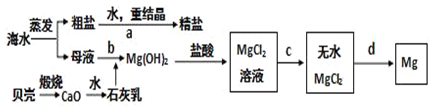
| A. | 步骤①、③的操作分别是过滤、萃取 | |
| B. | 步骤②的反应是非氧化还原反应 | |
| C. | 步骤③中加入的有机溶剂是裂化汽油或四氯化碳 | |
| D. | 步骤④的操作是过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
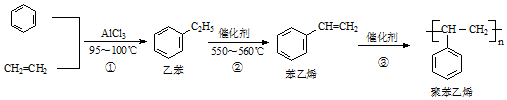
| A. | 苯乙烯的分子式为C8H8 | |
| B. | 1mol苯乙烯最多可与4molH2发生加成反应 | |
| C. | 鉴别乙苯与苯乙烯可用Br2的四氯化碳溶液 | |
| D. | 乙烯、苯和乙苯的分子中所有原子均可处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com