
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.标准状况下,22.4L苯所含有的分子数为NA
B.1mol羟基中含有的电子数为10NA
C.14g C2H4和C3H6混合气体含有的原子数为3NA
D.1L0.1mol/L的醋酸溶液中含有H+个数为0.1NA
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】由NO2、O2和熔融NaNO3组成的燃料电池如图所示。在该电池工作过程中石墨Ⅰ电极产生一种气态氧化物Y。下列说法正确的是( )

A.Y可能为NO B.电流由石墨Ⅰ流向负载
C.石墨Ⅰ上发生还原反应 D.石墨Ⅱ上的电极反应:O2+2N2O5+4e-=4NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)又叫乙二酸,广泛存在于植物源食品中,25℃时,其解离常数Kal=5.9×10-2; Ka2= 6.4×10-5。下列与草酸有关的说法错误的是
A.H2C2O4(aq) H+(aq) +HC2O4-(aq) △H >0;升温有利于提高草酸的电离程度
B.草酸中的碳为+3价,具有较强的还原性,可使酸性高锰酸钾溶液褪色
C.25℃时,KHC2O4溶液呈弱酸性,有时用于清洗金属表面的锈迹
D.同浓度的KHC2O4和K2C2O4混合溶液中:2c( H2C2O4) +2c( HC2O4)+2c( C2O42-) =3c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期p区元素多为非金属元素
(1)基态磷原子的价层电子排布图是__________,第三周期元素中,第一电离能最大的前三种元素是__________________。
(2)BF3、NF3、PCl3、SCl2四种分子中,属于平面三角形的是____________,中心原子杂化类型为sp3的是_______________。
(3)已知H2O的沸点比H2O2低58℃但比H2S高160℃,导致这种差异的原因是________________。
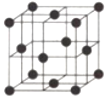
(4)金属铝的晶胞结构如图,若晶胞参数r pm,则单质的密度为(用NA表示阿伏加德罗常数)_______________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaN3是一种易溶于水(NaN3=Na++N3-)的白色固体,可用于有机合成和汽车安全气囊的产气药等。钠法(液氨法)制备NaN3的工艺流程如下:
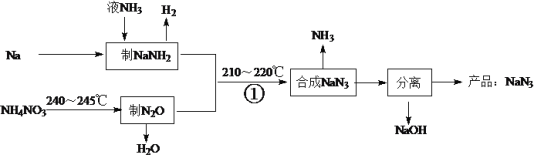
(1)钠元素在周期表中的位置是______________。
(2)NaN3中含有的化学键类型为_________________________________。
(3)NaNH2中氮元素的化合价为__________________。
(4)反应NH4NO3![]() N2O↑+2H2O↑中,每生成0.25molN2O转移电子数约_____个。
N2O↑+2H2O↑中,每生成0.25molN2O转移电子数约_____个。
(5)销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为_______(N3-被氧化为N2)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸的结构简式如图所示,下列关于莽草酸的说法正确的是( )

A.可用溴水鉴别莽草酸、乙醇、四氯化碳和苯
B.1mol莽草酸在催化剂条件下与2mol H2发生加成反应
C.分子中含有2种官能团
D.水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图,下列关于该有机物的说法正确的是( )

A.1 mol 该有机物可消耗 3 mol NaOHB.该有机物的分子式为 C16H17O5
C.最多可与 8 mol H2 发生加成D.苯环上的一溴代物有 6 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为几种晶体或晶胞的示意图:
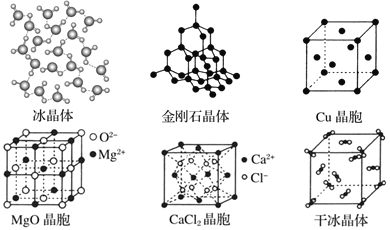
请回答下列问题:
(1)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_____。
(2)MgO晶体中,距每个O2-最近且距离相等的O2-有_____个。
(3)每个Cu晶胞中实际占有_____个Cu原子;CaCl2晶体中Ca2+的配位数为_____。
(4)冰的熔点远高于干冰,除 H2O 是极性分子、CO2 是非极性分子外, 还有一个重要的原因是____。
(5)金刚石晶胞含有_________个碳原子;若碳原子半径为 r,根据硬球接触模型,列式表示碳原子在晶胞中的空间占有率_____(计算结果为含π的分数,不要化为小数或百分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
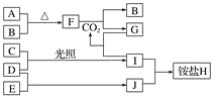
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com