
 ��
��| ��Ŀ | ���ȱ� | �Ȼ�β�� | ���� | ��Ʒ | ��ȷ������ | �ϼ� |
| ����ʧ����t/kg�� | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
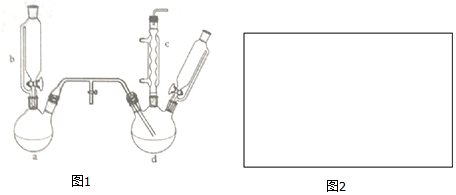
���� ��1��������غ��ظ�����Ʊ��������ü��ȣ�
��2����Ӧ��C���ȿ��Ʒ�Ӧ�¶���40-60�棬Ӧ����ˮԡ���ȣ�
��3��������������cΪ���������ܣ����ڱ��ӷ�����Ӧ������HCl������δ��Ӧ��������������c���ڵ�����
��4���ɱ��������ڴ�������������ȡ�ȱ���
��5����d�з�Ӧ��ɺ���l3��HCl�ȸ���Ʒ��������ˮ��
���ܽ���������������Ʒ�����Ӧ��
��6������Ũ��������ˮ������
��7�����ݱ�������ʧ������μӷ�Ӧ�ı����������ٸ��ݱ����ȱ��������ȹ�ϵ���㣮
��� �⣺��1������������������Ҫ���ȣ�������غ��ظ���ز��ã�
�ʴ�Ϊ��BC��
��2����Ӧ��C���ȿ��Ʒ�Ӧ�¶���40-60�棬Ӧ����ˮԡ���ȣ�
�ʴ�Ϊ��ˮԡ���ȣ�
��3������cΪ���������ܣ����ڱ��ӷ�����Ӧ������HCl������δ��Ӧ��������D���������к���HCl����������������
�ʴ�Ϊ�������Σ������ܣ���������
��4����ȡ�ȱ��Ļ�ѧ����ʽΪ��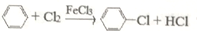 ��
��
�ʴ�Ϊ��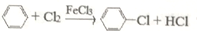 ��
��
��5����d�з�Ӧ��ɺ���l3��HCl�ȸ���Ʒ��������ˮ����ϴ֮ǰҪˮϴ������ϴȥ��Щ�����Լ������������ͳɱ���
�ʴ�Ϊ��ϴȥFeCl3��HCl�������ʡ������������ͳɱ���
�ڴ����Ȼ������������Ʒ�Ӧ������HCl�����������Ʒ�Ӧ���ܽ������Ҳ�����������Ʒ�Ӧ���÷�ӦΪ������ԭ��Ӧ��Cl2+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ��Cl2+2NaOH=NaCl+NaClO+H2O��
��6��Ũ�������������ˮ������Ϊ������գ�������Ӧ�����̳���װ��Ϊ��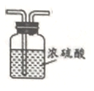 ��
��
�ʴ�Ϊ�� ��
��
��7����������ʧ��Ϊ89.2Kg/t����1t���вμӷ�Ӧ�ı�������Ϊ��1t-0.0892t�����ɱ����ȱ�����֮��Ϊ78��112.5����10t �����Ƶó�Ʒ�ȱ�Ϊ��$\frac{10����1-0.0892����112.5}{78}$t��
�ʴ�Ϊ��$\frac{10����1-0.0892����112.5}{78}$��
���� ���⿼���л����Ʊ�ʵ�鷽�����漰��װ�á�������ԭ���ķ��������Լ���ѧ����ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д� �ľ�ͼ���ʱ�ȷ�ϵ�д�
�ľ�ͼ���ʱ�ȷ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���ʣ����ʣ� | �Լ� | ���� |
| A | CO2��SO2�� | ����Na2CO3��Һ | ϴ�� |
| B | NaCl��Һ��Na2CO3�� | BaCl2 | ���� |
| C | Cl2��HCl�� | ����NaCl��Һ | ϴ�� |
| D | KI��Һ��I2�� | �Ҵ� | ��ȡ��Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
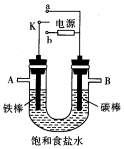 ������ͼװ�ý��е绯ѧ�����ʵ�飬�ش��������⣮
������ͼװ�ý��е绯ѧ�����ʵ�飬�ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
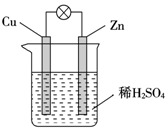
| A�� | ���Ӵ�ͭƬ�����·����п | B�� | ZnΪ������CuΪ���� | ||
| C�� | H+��ͭƬ�ϵõ��ӷ���������Ӧ | D�� | ��װ���ܽ�����ת��Ϊ��ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȡһ�������壬�ܽ⣬����Һ�м�������CaO��ĩ����ַ�Ӧ��۲쵽�а�ɫ�������ɣ�˵��ԭ������һ������Na2CO3 | |
| B�� | ȡһ�������壬�ܽ⣬����Һ��ͨ���CO2���۲쵽�о���������˵��ԭ������һ������Na2CO3 | |
| C�� | ȡһ�������壬���ȣ���������������ʹ����ʯ��ˮ����ǣ�˵��ԭ������һ������NaHCO3 | |
| D�� | ȡһ�������壬�μ�0��l mol/L������1Lʱ����Һ�����ԣ�˵�������и����ʵ����ʵ����ܺ�Ϊ0.05 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶ȣ��淴Ӧ���ʼӿ죬����Ӧ���ʼ��� | |
| B�� | ʹ�ô����Ȳ�ʹ�ô�����ѧƽ�ⳣ��Ҫ�� | |
| C�� | ����������ԭ����֪�ϳɰ�ʱ�������NH3�������ԭ�������� | |
| D�� | ��ѹ�ܼӿ췴Ӧ���ʣ���Ϊ�����˻���Ӱٷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��N3-�ĵ��Ӳ�ṹ�����ԭ����ͬ | |
| B�� | Na3N�е�Na+�İ뾶����N3-�İ뾶 | |
| C�� | Na3N�����ᷴӦ������������ | |
| D�� | Na3N��ˮ�ķ�Ӧ����������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com