
【题目】2molA与2molB混合于2L的密闭容器中,发生如下反应,2A(g)+3B(g) ![]() 2C(g)+2D(g),2s后A的转化率为50%,测得v(D)=0.25mol/(L·s)。下列推断不正确的是
2C(g)+2D(g),2s后A的转化率为50%,测得v(D)=0.25mol/(L·s)。下列推断不正确的是
A. z=2
B. 2s后,容器内的压强是初始的7/8倍
C. 2s时,C的体积分数为2/7
D. 2s后,B的浓度为0.5mol/L
【答案】D
【解析】试题分析:2s后A的转化率为50%,则反应的A为2mol×50%=1mol,则
2A(g)+3B(g)2C(g)+zD(g),
开始2 2 0 0
转化1 1.5 1 0.5z
2s 1 0.5 1 0.5z
A.v(A)=1mol/2L÷2s=0.25molL-1s-1=v(D),因反应速率之比等于化学计量数之比,z=2,故A正确;B.2s后,容器内的物质的量总和是 1+0.5+1+0.5×2=3.5mol,恒温恒容条件下,压强与物质的量成正比,2s后反应内的压强是反应前的3.5mol/4mol=7/8倍,正确;C.2s后C的体积分数为1mol/3.5mol=2/7,正确;D.2s后,B的浓度为0.5mol/2L=0.25mol/L,错误;答案为D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】利用下图装置进行实验,甲乙两池均为1 mol·L–1的AgNO3溶液,A、B均为Ag电极。实验开始先闭合K1,断开K2。一段时间后,断开K1,闭合K2,形成浓差电池,灵敏电流计指针发生偏转(提示:Ag+ 浓度越大,氧化性越强)。下列说法不正确的是( )

A. 闭合K1,断开K2后,A电极增重
B. 闭合K1,断开K2后,乙池溶液中Ag+浓度增大
C. 断开K1,闭合K2后,NO3–向A电极移动
D. 断开K1,闭合K2后,B电极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液是用稀硝酸腐蚀锌板后得到的 ,某化学兴趣小组拟用该废液(含有少量的 Cl-、Fe3+)制取 Zn(NO3)2·6H2O 的过程如下:
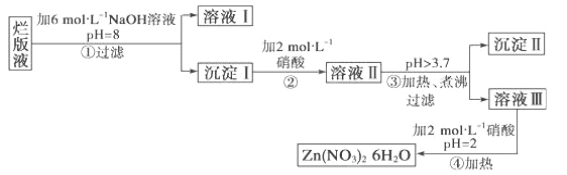
已知:Zn(NO3)2·6H2O 是一种无色晶体,水溶液呈酸性,Zn(NO3)2 能与碱反应,得到的产物 Zn(OH)2 具有
两性,Fe3+在 PH=3.7 时就能完全沉淀。
(1)该废液溶质的主要成分是______(填化学式)。
(2)在操作①中保持 pH=8 的目的是__________________________________________。
(3)沉淀Ⅰ的成分是________________________________________。
(4)操作③中加热、煮沸的目的是______________________________________;
(5)操作④保持 pH=2 的目的是_________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国晋代炼丹家、医学家葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银,积变又成丹砂”。这句话所指的是:①红色的硫化汞(即丹砂,化学式为HgS)在空气中灼烧有汞生成;②汞和硫在一起研磨生成黑色硫化汞;③黑色硫化汞隔绝空气加热变成红色硫化汞晶体。
(1)在上述三点含义中,描述的______(填“有”或“无”)物理变化,若有的话,请写出哪些?并说明理由______(填序号),理由是______。
(2)在上述三点含义中,描述的______(填“有”或“无”)化学变化,若有的话,请写出哪些?并写出反应的文字表达式:_______、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度晶硅是典型的无机非金属材料,又称“半导体”材料.它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:

下列说法不正确的是
A. 步骤①的化学方程式为:SiO2+C![]() Si+CO2↑
Si+CO2↑
B. 步骤①中每生成1mol Si,转移4mol电子
C. 高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
D. SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用石墨烯和具有粘弹性的聚硅树脂(俗称橡皮泥)制备出一种具有极高灵敏度的电力学传感材料,能够检测轻微的变形和冲击,其灵敏程度甚至能探测到蜘蛛的运动。该材料可用于制作检测人体脉搏、血压的传感器等。实验室模拟工业合成方法,制备聚硅树脂的中间体氯甲基三乙氧基硅烷ClCH2Si(OEt)3 。量取20mL甲基三氯硅烷(CH3SiCl3)注入三颈烧瓶中,开启电磁搅拌加热器升温至66℃,从a中加入浓盐酸,加热A一段时间,待温度升至110℃,停止加热,在三颈烧瓶中加入30mL无水乙醇(EtOH),迅速反应生成氯甲基三乙氧基硅烷ClCH2Si(OEt)3,待温度降至室温后,将三颈烧瓶中液体转移到蒸馏烧瓶中蒸馏,收集得到174.5℃馏分12mL。
物质 | C2H5OH | CH3SiCl3 | ClCH2SiCl3 | ClCH2Si(OEt)3 |
相对分子质量 | 46 | 149.5 | 184 | 212.5 |
熔点/℃ | -114.1 | -77.8 | — | — |
沸点/℃ | 78.3 | 66.4 | 116.5 | 174 |
密度/g·mL | 0.79 | 1.30 | 1.47 | 1.02 |
已知:①甲基三氯硅烷为无色液体,具有刺鼻恶臭,易潮解;氯甲基三乙氧基硅烷易水解,能与碱金属氢氧化物生成碱金属硅醇盐。②CH3CH2OH也可简写成EtOH
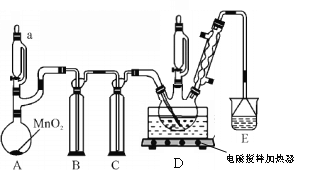
(1)连接好装置后,检验装置气密性的操作是:D和E之间夹上止水夹,B中装入适量蒸馏水,___________________________________________________说明装置气密性完好。
(2) A装置中发生反应的离子方程式是:_______________________;装置C的作用是:_______________________ ;E中所装液体是:__________________;
(3)装置D中发生反应的化学方程式为:① CH3SiCl3 + Cl2 → ClCH2SiCl3 + HCl
②___________________________________________________________;球形冷凝管的作用是:________________________;
(4) 有同学发现该装置有一处不足可能会导致实验失败,应该___________________;
(5) 该方法制备氯甲基三乙氧基硅烷的产率(实际产量/理论产量)是:_______________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置a、b、c中分别盛有试剂1、2、3,用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓 | Cu片 | KI-淀粉溶液 | 验证 |
|
B | 盐酸 | 石灰石 | 饱和 | 制备 | |
C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证溶液X中是否有 | |
D | 70%硫酸 |
| 酸性 | 证明 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A. 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3,其中c(CO32-)的大小关系为:②>④>③>①
B. pH=2 的H2C2O4溶液与pH=12 的NaOH 溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C. 向0.2mo/L 的NaHCO3 溶液中加入等体积0.1mo/L 的NaOH 溶液:c(CO32- )>c(HCO3-)>c(OH-)>c(H+)
D. 常温下,等浓度的CH3COOH与CH3COONa 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(H+)+c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com