

分析 (一)碳酸钙的制备
由流程可知,加盐酸,碳酸钙、铁的氧化物均溶解,加双氧水可氧化亚铁离子,加氨水将铁离子转化为沉淀,过滤后的滤液中含盐酸,加氨水中和酸,利用得到碳酸钙沉淀;
(1)碱可中和酸,小火煮沸利于沉淀生成;
(二)过氧化钙的制备
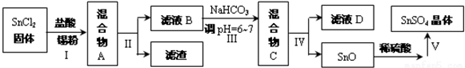
由流程可知,碳酸钙溶于盐酸后,至溶液中尚存有少量固体,过滤后,滤液中氯化钙、氨水、过氧化氢反应生成CaO2、NH4Cl、水;再过滤,洗涤得到过氧化钙;制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品,石灰石便宜易得,但纯度较低,以此来解答.
解答 解:(一)碳酸钙的制备
由流程可知,加盐酸,碳酸钙、铁的氧化物均溶解,加双氧水可氧化亚铁离子,加氨水将铁离子转化为沉淀,过滤后的滤液中含盐酸,加氨水中和酸,利用得到碳酸钙沉淀;
(1)步骤①加入氨水的目的是中和多余的盐酸,沉淀铁离子.小火煮沸的作用是使沉淀颗粒长大,有利于过滤,
故答案为:调节溶液pH使Fe(OH)3沉淀;过滤分离;
(二)过氧化钙的制备
由流程可知,碳酸钙溶于盐酸后,至溶液中尚存有少量固体,过滤后,滤液中氯化钙、氨水、过氧化氢反应生成CaO2、NH4Cl、水;再过滤,洗涤得到过氧化钙;
(2)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,溶液中溶解二氧化碳,此时溶液呈酸性;将溶液煮沸,趁热过滤,将溶液煮沸的作用是除去溶液中溶解的二氧化碳,
故答案为:酸;除去溶液中溶解的二氧化碳;
(3)步骤③中反应的化学方程式为CaCl2+2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl 或CaCl2+2NH3•H2O+H2O2=CaO2↓+2NH4Cl+2H2O,该反应需要在冰浴下进行,原因是温度过高时双氧水易分解,
故答案为:CaCl2+2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl 或CaCl2+2NH3•H2O+H2O2=CaO2↓+2NH4Cl+2H2O;温度过高时双氧水易分解;
(4)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是去除晶体表面水分,
故答案为:去除晶体表面水分;
点评 本题考查物质的制备实验,为高频考点,把握制备实验原理、实验技能、物质的性质为解答的关键,侧重分析与实验能力的考查,注意物质的性质及应用,题目难度中等.


科目:高中化学 来源: 题型:解答题
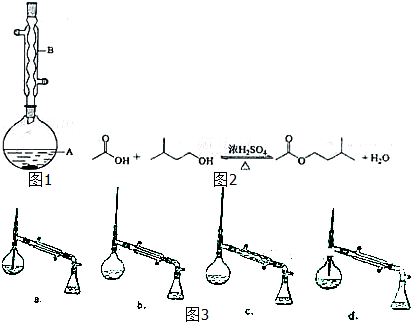
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
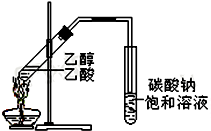 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
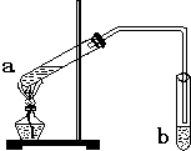 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
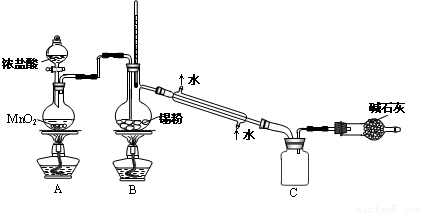
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
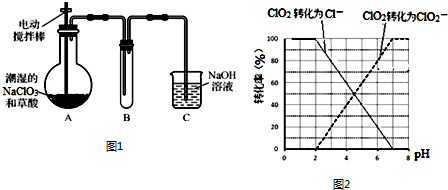
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=+244.1kJ/mol | B. | △H=-488.3kJ/mol | C. | △H=-996.6kJ/mol | D. | △H=+996.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | +1940 kJ•mol-1 | B. | -1940 kJ•mol-1 | C. | -485 kJ•mol-1 | D. | +485 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1,则H2燃烧热为241.8 kJ•mol-1 | |
| B. | 从C(石墨,s)═C(金刚石,s)△H=+1.9 kJ/mol,可知:金刚石比石墨更稳定 | |
| C. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 | |
| D. | 化学反应中的能量变化,通常表现为热量的变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com