
【题目】某学生利用以下装置探究氯气与氨气之间的反应。其中C为纯净干燥的氯气与氨气反应的装置。请回答下列问题:
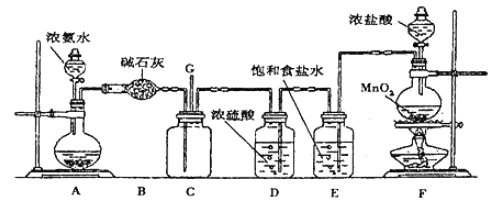
(1)装置A中的烧瓶内固体不能选用_____________。
A.生石灰 B.碱石灰
C.五氧化二磷 D.烧碱
(2)装置A中发生反应的化学方程式为________________________。
(3)B装置的作用_____________;E装置的作用_____________。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式:___________。
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,需要处理,写出离子方程式________________;
实验室制备氨气,下列方法中适宜选用的是________________________。
①固态氯化铵加热分解
②浓氨水中加入固体氢氧化钠
③加热浓氨水
④固态氯化铵与氢氧化钙混合加热
【答案】C NH3·H2O ![]() NH3↑+H2O 干燥气体 吸收HCl 8NH3+3Cl2=N2+6 NH4Cl Cl2+2OH-=Cl-+C1O-+H2O ②③④
NH3↑+H2O 干燥气体 吸收HCl 8NH3+3Cl2=N2+6 NH4Cl Cl2+2OH-=Cl-+C1O-+H2O ②③④
【解析】
(1)五氧化二磷为酸性氧化物与氨气反应,故不能选用;
(2)装置A中一水合氨分解生成氨气;
(3)碱石灰可以干燥氨气,饱和食盐水可以除去氯气中的氯化氢杂质;
(4)氨气和氯气反应生成氯化铵和氮气;
(5)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
①加热氯化铵生成氨气和氯化氢,氨气和氯化氢遇冷又生成氯化铵;
②固体氢氧化钠溶于水放热,电离产生氢氧根离子,结合一水合氨电离平衡移动影响因素;
③一水合氨受热分解生成氨气;
④固态氯化铵与氢氧化钙混合加热生成氨气。
(1)生石灰与水反应生成氢氧化钙,放出大量的热,有利于氨气的逸出;氢氧化钠溶于水放热,促使氨水分解,且OH-的浓度增大有利于NH3的生成,所以可以用将浓氨水逐滴滴加到生石灰、碱石灰或烧碱上制取氨气,五氧化二磷为酸性氧化物与氨气反应,故不能选用,
故答案选C;
(2)装置A中一水合氨分解生成氨气,化学方程式为NH3·H2O ![]() NH3↑+H2O,
NH3↑+H2O,
故答案为:NH3·H2O ![]() NH3↑+H2O;
NH3↑+H2O;
(3)B装置中,可以用碱石灰干燥氨气,E装置中,可以用饱和食盐水除去氯气中的氯化氢杂质;
故答案为:干燥气体;除去氯气中的氯化氢;
(4)氨气和氯气反应生成白烟氯化铵和空气的主要成分之一氮气,即反应的化学方程式为8NH3+3Cl2═6NH4Cl+N2;
故答案为:8NH3+3Cl2═6NH4Cl+N2;
(5)氯气是酸性气体,可以用氢氧化钠来进行尾气处理,反应的离子方程式为Cl2+2OH-=Cl-+C1O-+H2O,
故答案为:Cl2+2OH-=Cl-+C1O-+H2O;
①加热氯化铵生成氨气和氯化氢,氨气和氯化氢遇冷又生成氯化铵,不能制得氨气,故①错误;
②固体氢氧化钠溶于水放热,电离产生氢氧根离子,氢氧根离子浓度增大,抑制了NH3·H2O的电离,有利于氨气的逸出,故②正确;
③一水合氨受热分解生成氨气,故③正确;
④固态氯化铵与氢氧化钙混合加热生成氨气,能够制得氨气,故④正确;
故选:②③④。


科目:高中化学 来源: 题型:
【题目】高分子材料尼龙66具有良好的抗冲击性、韧性、耐燃油性和阻燃、绝缘等特点,因此广泛应用于汽车、电气等工业中。以下是生产尼龙66的一些途径。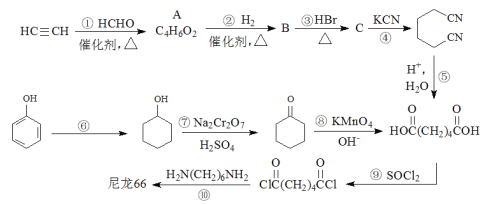
(1)A中所有碳原子都处于同一直线上,则A的结构简式为_____________。
(2)B的名称是_____________。
(3)反应①~④中,属于加成反应的有_____________,反应⑥~⑨中,属于氧化反应的有_____________。
(4)请写出反应⑥的化学方程式为_____________。
(5)高分子材料尼龙66中含有![]() 结构片段,请写出反应⑩的化学方程式为_____________。
结构片段,请写出反应⑩的化学方程式为_____________。
(6)某聚合物K的单体与A互为同分异构体,该单体核磁共振氢谱有三个峰,峰面积之比为1:2:3,且能与NaHCO3溶液反应,则聚合物K的结构简式是_____________。
(7)聚乳酸( )是一种生物可降解材料,已知羰基化合物可发生下述反应:
)是一种生物可降解材料,已知羰基化合物可发生下述反应: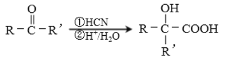 (R′可以是烃基或H原子)。用合成路线图表示用乙醇制备聚乳酸的过程_____________。
(R′可以是烃基或H原子)。用合成路线图表示用乙醇制备聚乳酸的过程_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是
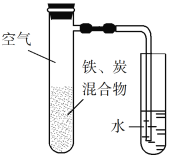
A. 铁被氧化的电极反应式为Fe3e![]() Fe3+
Fe3+
B. 铁腐蚀过程中化学能全部转化为电能
C. 活性炭的存在会加速铁的腐蚀
D. 以水代替NaCl溶液,铁不能发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量X气体通入Y溶液中,实验结果与预测现象一致的组合是( )
X气体 | Y溶液 | 预测现象 |
| |
① | CO2 | Na2SiO3溶液 | 有白色沉淀产生 | |
② | SO2 | BaCl2溶液 | 有白色沉淀产生 | |
③ | Cl2 | AgNO3溶液 | 有白色沉淀产生 | |
④ | NH3 | AlCl3溶液 | 有白色沉淀产生 |
A.只有①②③B.只有①②④
C.只有①③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
NaHCO3+H2![]() HCOONa+H2O下列有关说法正确的是
HCOONa+H2O下列有关说法正确的是
A. 储氢、释氢过程均无能量变化
B. NaHCO3、HCOONa均含有离子键和共价键
C. 储氢过程中,NaHCO3被氧化
D. 释氢过程中,每消耗0.1molH2O放出2.24L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷与氧气反应过程中的能量变化如下图所示。下列有关说法中正确的是

A. 反应 CO2(g)+2H2O(l)==CH4(g)+2O2(g) △H<0
B. 若将1mol CO2(g)、2 molH2O(l)的能量标在图中,则其位置在①、②之间
C. 若C一H键的键能为415kJ mol-1,则O= O的键能为493 kJ mol-1
D. 若该反应过程中转化的化学能为200kJ,则有0.25 molC=O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物G是一种治疗胃及十二指肠溃疡、反流性或糜烂性食管炎等的药物,G 的一种合成路线如下:
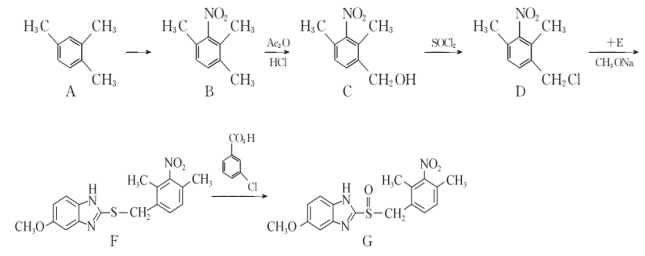
回答下列问题:
(1)A的化学名称为____________,C中所含官能团名称为____________。
(2)C生成D的反应类型为____________,F生成G的反应类型为____________。
(3)由A生成B的化学方程为____________。
(4)E的分子式为C8H8ON2S,其结构简式为____________。
(5)芳香化合物W是C的同分异构体。满足下列条件的W共有_________种(不含立体异构)。
①W分子中含氨基、羧基和羟基三种官能团
②苯环上只有两个取代基
③能与FeCl3溶液发生显色反应
其中核磁共振氢谱显示有6种不同化学环境的氢的结构简式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】400 ℃时,将一定量的SO2和14 mol O2压入一个盛有催化剂的10 L密闭容器中进行反应:2SO2+O2![]() 2SO3,已知2 min后,容器中剩余2 mol SO2和12 mol O2。试计算:
2SO3,已知2 min后,容器中剩余2 mol SO2和12 mol O2。试计算:
(1)生成SO3的物质的量__________________。
(2)SO2的起始物质的量浓度____________________。
(3)2 min内SO2和SO3的反应速率______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中产生的现象与对应的图形相符的是( )
A.  NaHSO3 粉末加入HNO3溶液中B.
NaHSO3 粉末加入HNO3溶液中B.  SO2气体通入新制氯水中
SO2气体通入新制氯水中
C.  NaOH溶液滴入 Ba(HCO3)2溶液中D.
NaOH溶液滴入 Ba(HCO3)2溶液中D. 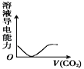 CO2气体通入澄清石灰水中
CO2气体通入澄清石灰水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com