
| A、1173 kJ |
| B、1456 kJ |
| C、2022 kJ |
| D、2346 kJ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
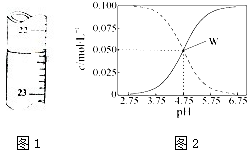 (1)用0.1026mol?L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图1所示,此时的读数为
(1)用0.1026mol?L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图1所示,此时的读数为
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸馏 | B、分液 | C、过滤 | D、萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、定容时,仰视标线 |
| B、摇匀后,发现容量瓶中水低于刻度线,再加水 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、NaOH固体溶解后,溶液未经冷却就立即移液至容量瓶中并定容 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com