
| 6.72L |
| 22.4L/mol |
| 62g×0.1mol |
| 2mol |


科目:高中化学 来源: 题型:
 TiO2俗称钛白粉,用途广泛,现正广泛开发,将来有机会成为新工业.工业上利用TiO2制备金属钛的流程如下.
TiO2俗称钛白粉,用途广泛,现正广泛开发,将来有机会成为新工业.工业上利用TiO2制备金属钛的流程如下.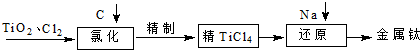
| 物质 | TiCl4 | FeCl3 | SiCl4 | AlCl3 |
| 沸点/℃ | 136 | 310 | 56.5 | 180 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙炔 | B、丙炔 |
| C、2-戊炔 | D、1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中加入硝酸银,产生白色沉淀,则溶液中可能含有Cl- |
| B、用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色,则溶液中一定有Na+,可能有K+ |
| C、加入稀盐酸产生能使澄清石灰水变浑浊的无色无味的气体,说明原溶液一定含有CO32- |
| D、可用焰色反应可区分KCl和NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al(OH)3能与NaOH溶液反应,则Al(OH)3也能与氨水反应 |
| B、过氧化钠能与二氧化碳反应产生氧气,可用作高空飞行或潜水的供氧剂 |
| C、Fe(OH)3溶于氢碘酸的离子方程式为Fe(OH)3+3H+═Fe3++3H2O |
| D、等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 离子组 | 评价 |
| A | H+、Mg2+、Br-、NO3- | 能大量共存于同一溶液中,投入少量锌粉后,可放出H2 ,反应的离子方程式为 Zn+2H+=Zn2++H2↑ |
| B | NH4+、CO32-、Cl-、Al3+ | 不能大量共存于同一溶液中,因为有沉淀生成 2Al3++3CO32-=Al2(CO3)3↓ |
| C | ClO-、Na+、K+、HSO3- | 能大量共存于同一溶液中 |
| D | HCO3-、OH-、Na+、K+ | 不能大量共存于同一溶液中,因为发生如下反应 HCO3-+OH-=CO32-+H2O |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示.请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com