
【题目】完成下列有关物质的量的计算
(1)![]() 个
个![]() 分子的物质的量是________
分子的物质的量是________![]() 。
。
(2)标准状况下,![]() 的体积是_________L。
的体积是_________L。
(3)含有相同氧原子数的![]() 和
和![]() ,其分子的质量比为_________。
,其分子的质量比为_________。
(4)标准状况下,![]() 气体溶于水配制成
气体溶于水配制成![]() 溶液,其物质的量浓度为_______
溶液,其物质的量浓度为_______![]() 。
。
(5)![]() 碳在一定量的氧气中完全燃烧,反应后生成
碳在一定量的氧气中完全燃烧,反应后生成![]() 和
和![]() 混合气体的平均摩尔质量是
混合气体的平均摩尔质量是![]() ,则生成的
,则生成的![]() 的质量是_____
的质量是_____![]() 。
。
【答案】0.2 44.8 6:5 ![]() 6.3
6.3
【解析】
(1)根据n=![]() 计算;
计算;
(2) 根据n=![]() =
=![]() 分析计算;
分析计算;
(3) 根据n=![]() =
=![]() 结合分子构成判断;
结合分子构成判断;
(4) 根据n=![]() ,再结合c=
,再结合c=![]() 计算;
计算;
(5)依据n=![]() 计算碳物质的量,结合碳元素守恒可知二氧化碳和一氧化碳物质的量与碳物质的量相同,根据摩尔质量概念计算。
计算碳物质的量,结合碳元素守恒可知二氧化碳和一氧化碳物质的量与碳物质的量相同,根据摩尔质量概念计算。
(1)n=![]() =
=![]() 0.2mol,
0.2mol,![]() 分子的物质的量是0.2mol;
分子的物质的量是0.2mol;
(2)![]() 的物质的量=
的物质的量=![]() =2mol,标准状况下,体积=2mol ×22.4L/mol=44.8L;
=2mol,标准状况下,体积=2mol ×22.4L/mol=44.8L;
(3)含有相同氧原子数的SO2和SO3,物质的量之比为3:2,则分子质量之比为3×64:2×80=6:5;
(4)标准状况下,![]() 气体的物质的量=
气体的物质的量=![]() =
=![]() ,溶于水配制成
,溶于水配制成![]() 溶液,其物质的量浓度为
溶液,其物质的量浓度为![]() =
=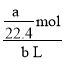 =
=![]()
![]() ;
;
(5) 3.6g碳物质的量=![]() =0.3mol,反应后生成CO和CO2混合气体物质的量为0.3mol,混气体平均摩尔质量是32g/mol,则混合气体质量=32g/mol×0.3mol=9.6g,设一氧化碳物质的量为x,二氧化碳物质的量为(0.3x)mol,28x+44(0.3x)=9.6,x=0.225mol,一氧化碳质量=0.225mol×28g/mol=6.3g。
=0.3mol,反应后生成CO和CO2混合气体物质的量为0.3mol,混气体平均摩尔质量是32g/mol,则混合气体质量=32g/mol×0.3mol=9.6g,设一氧化碳物质的量为x,二氧化碳物质的量为(0.3x)mol,28x+44(0.3x)=9.6,x=0.225mol,一氧化碳质量=0.225mol×28g/mol=6.3g。


科目:高中化学 来源: 题型:
【题目】某固体混合物X,含有![]() 、
、![]() 、
、![]() 和
和![]() 中的几种,进行如下实验:
中的几种,进行如下实验:
①X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z;
②沉淀Y与![]() 溶液作用,无变化。
溶液作用,无变化。
下列说法不正确的是( )
A.混合物X中必定含有![]() ,不含
,不含![]()
B.溶液Z中溶质主要是钠盐,且必含![]()
C.灼烧沉淀Y,可能得到黑色物质
D.往溶液Z中加入Cu粉,若不溶解,说明X中不含![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列A、B、C、D是中学常见的混合物分离或提纯的基本装置:
A.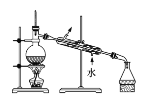 B.
B.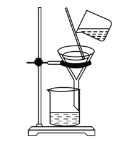 C.
C.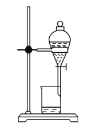 D.
D.
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置,将A、B、C、D填入适当的空格中
(1)除去粗盐水中的泥沙:__________;
(2)与海水晒盐原理相似的是__________;
(3)用四氯化碳从碘水中提取碘:__________;
(4)分离![]() (沸点:
(沸点:![]() )和苯(沸点:
)和苯(沸点:![]() )的混合物(互溶)__________。
)的混合物(互溶)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)乙醇(CH3CH2OH)在PMR(核磁共振氢谱)中可能有__________组信号峰,甲醚(CH3OCH3)在PMR(核磁共振氢谱)中可能有__________组信号峰。
(2)在常温下测得的某烃C8H10的PMR(核磁共振氢谱),观察到两种氢原子给出的信号,其强度之比为2∶3,试确定该烃的结构简式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)有X、Y、Z三种短周期元素,原子半径大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质分子在适当条件下可发生如图变化,其中B和C均为10电子分子.下列说法中不正确的是
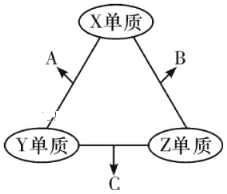
A. X与Z形成的某种化合物可用来杀菌消毒 B. C极易溶于B中,溶液呈碱性
C. Y与Z形成的二元化合物只含有极性键 D. A和C能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强热条件下,硫酸亚铁固体可发生如下反应:2FeSO4![]() Fe2O3+SO2↑+SO3↑。若将此反应生成的气体先通入足量BaCl2溶液,再通入品红溶液中,则可能的现象为( )
Fe2O3+SO2↑+SO3↑。若将此反应生成的气体先通入足量BaCl2溶液,再通入品红溶液中,则可能的现象为( )
①BaCl2溶液中无沉淀析出;
②析出BaSO3沉淀;
③析出BaSO4沉淀;
④品红溶液褪色;
⑤品红溶液不褪色;
A.①④B.②④C.②③⑤D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系:A![]() B
B![]() C
C![]() D,且D为强酸或强碱(其它相关物质可能省略)。下列说法不正确的是( )
D,且D为强酸或强碱(其它相关物质可能省略)。下列说法不正确的是( )
A.若A为非金属单质,则D一定为硝酸或硫酸
B.若A为金属单质,则A一定位于第三周期ⅠA族
C.若A是共价化合物,A的水溶液一定能显碱性
D.不论A是单质还是化合物,D都有可能是同一种物质,其浓溶液在常温下都能使铁和铝发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A.某温度下,1 L pH = 6 的纯水中含 OH一为10-8mol
B.25℃ 时,向0. 1 mo lL-1 CH3COONa 溶液中加入少量水,溶液中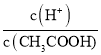 减小
减小
C.25℃时,将 V1 L pH = 11的 NaOH溶液与V2 L pH = 3 的H A 溶液混合,溶液显中性,则V1 ≤V2
D.25℃时,将 a molL-1 氨水与0.01 molL- 1 盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),用含a的代数式表示 NH3H2O)的电离常数 Kb = ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为2mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法正确的是( )
A.该溶液中所含的离子是:Fe2+、Al3+、SO42-、NO3-
B.若向该溶液中加入过量的稀硫酸,产生的气体分子数为1/3NA
C.若向该溶液中加入过量的稀硫酸后若再滴加FeCl2溶液,没有现象
D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为160g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com