
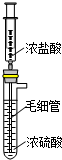
 实验室用如图装置制备HCl气体.
实验室用如图装置制备HCl气体.
分析 (1)浓硫酸吸水,放出大量的热,有利于HCl的逸出;
(2)由量取混合酸体积精度,可以选择酸式滴定管量取,由配制溶液体积可知在500mL容量瓶中定容;
装瓶前用标准溶液对试剂瓶进行润洗,避免滴定液被稀释,引起实验误差;
标签应注明物质的量浓度,根据n=$\frac{m}{M}$计算氢氧化钡物质的量,再根据c=$\frac{n}{V}$计算氢氧化钡溶液浓度;
(3)用标准Ba(OH)2溶液滴定至溶液由无色变为红色才停止滴定,出现这种情况的补救措施除重做外,还有可以采取的措施是:用待测酸液滴定至溶液立即由红色变为浅红色(且半分钟不褪色);
(4)反应生成硫酸钡沉淀,进行过滤、洗涤、干燥,称量硫酸钡的质量,恒重时可得硫酸钡质量,根据硫酸根守恒可以计算硫酸的浓度,氢离子源于硫酸与HCl,结合氢氧根离子中和氢离子,可以计算HCl的物质的量浓度;
(5)硫酸转化为硫酸钡沉淀,根据硫酸钡的质量,由硫酸根守恒计算硫酸的物质的量.
解答 解:(1)浓硫酸吸水,放出大量的热,使HCl溶解度减小,有利于HCl的逸出,可制备少量干燥HCl气体,
故选:ab;
(2)由量取混合酸体积精度,可以选择酸式滴定管量取,由配制溶液体积可知在500mL容量瓶中定容;
装瓶前用标准溶液对试剂瓶进行润洗,避免滴定液被稀释,引起实验误差;
标签应注明物质的量浓度,氢氧化钡物质的量为$\frac{4.7880g}{171g/mol}$=0.02800mol,氢氧化钡溶液浓度为$\frac{0.02800mol}{0.25L}$=0.1120mol/L,
故答案为:酸式滴定管、500mL容量瓶;避免滴定液被稀释,引起实验误差;0.1120mol/L;
(3)用标准Ba(OH)2溶液滴定至溶液由无色变为红色才停止滴定,出现这种情况的补救措施除重做外,还有可以采取的措施是:用待测酸液滴定至溶液立即由红色变为浅红色(且半分钟不褪色),
故答案为:用待测酸液滴定至溶液立即由红色变为浅红色(且半分钟不褪色);
(4)反应生成硫酸钡沉淀,进行过滤、洗涤、干燥,称量硫酸钡的质量,恒重时可得硫酸钡质量,根据硫酸根守恒可以计算硫酸的浓度,氢离子源于硫酸与HCl,结合氢氧根离子中和氢离子,可以计算HCl的物质的量浓度,
故答案为:过滤、洗涤、干燥;恒重;
(5)硫酸转化为硫酸钡沉淀,根据硫酸钡的质量,由硫酸根守恒计算硫酸的物质的量,固体Ba(OH)2中混有少量的NaOH,不影响混合酸中硫酸浓度的测定结果,
故答案为:无影响.
点评 本题考查滴定原理的应用、一定物质的量浓度溶液配制等,属于定量实验,关键是对原理的理解,(2)中注意有效数字问题,难度中等.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
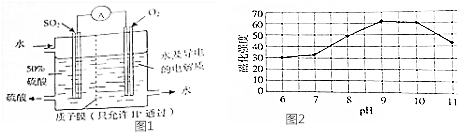
| 温度/℃ | 产品颜色 |
| 35 | 灰色 |
| 40 | 灰黑 |
| 60 | 黑色 |
| 65 | 红黑 |
| 80 | 黑褐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
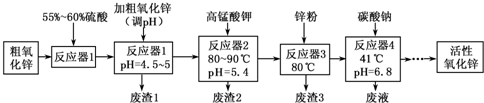
| Fe(OH)2 | Fe( OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
| 开始沉淀的pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| 沉淀完全的pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
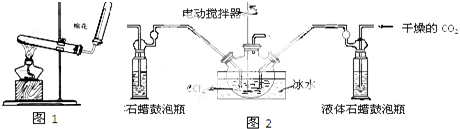
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2gO2、O3组成的混合物中含有的质子数为1.6NA | |
| B. | 当反应6HCl+KClO3═Cl2↑+KC1+3H2O有71gC l2生成时,转移电子数目为2NA | |
| C. | 1molC2H4分子中含共用电子对的数自为5NA | |
| D. | 0.1mol乙醇与足量乙酸充分反应后,生成的水分子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
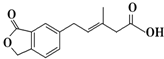
| A. | M可以发生加成、加聚、水解、酯化等反应 | |
| B. | 1mol M最多可以与3mol NaOH反应 | |
| C. | M苯环上的一氯取代物有三种不同结构 | |
| D. | 1mol M最多可以与5mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 | |
| C. | 同系物的分子量数值一定相差14的整数倍 | |
| D. | 同系物的化学性质相似,物理性质随碳原子数的递增呈现规律性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com