

���� ����ͼ1��֪���Ʊ����ƾ��������Ϊ����ˮâ����Na2SO4����̼�ڸ������շ�Ӧ��3Na2SO4+8C$\frac{\underline{\;����\;}}{\;}$3Na2S+4CO2��+4CO��������������ˮ�⣬����ϡ����Һ��������������ˮ�⣬ͨ�����ƻ�����ƾ��壬
��1������ͨ����Ϣȷ����Ӧ������Ȼ����ݡ����������ʵ�����CO��CO2�������ϼ۱仯���д����Ӧ�Ļ�ѧ����ʽ��
��2������������Һ��������ˮ���Լ��Ե�ˮ��ƽ��Ӱ�����ط����жϣ�
��3������ͼ�������߷�����ȥ�������PH��x��ȡֵ��
��4������ʱCuS��Cu��OH��2��Ksp�������ܶȻ���������õ���������ҺPH������Һ��ͭ����Ũ�ȣ�����CuS��Ksp����õ������ӵ�Ũ�ȣ�
��� �⣺�Ʊ����ƾ��������Ϊ����ˮâ����Na2SO4����̼�ڸ������շ�Ӧ��3Na2SO4+8C$\frac{\underline{\;����\;}}{\;}$3Na2S+4CO2��+4CO��������������ˮ�⣬����ϡ����Һ�������ղ����������Һ��ͨ�����ƻ�����ƾ��壬
��1�����������Ϣ����������̼��Ӧ���ɵ����ʵ�����CO��CO2��CԪ�ػ��ϼ۴�0�۱�������+4��+2�ۣ����ϼ���������Ϊ����4-0��+��2-0��=6����������+6��SԪ�ر���ԭΪ-2�ۣ����ϼ۽�����8�ۣ��ϼ۱仯����С������Ϊ24���������Ƶ�ϵ��Ϊ3��һ����̼��������̼��ϵ��Ϊ4��Ȼ����������غ㶨����ƽ����ƽ��Ļ�ѧ����ʽΪ��3Na2SO4+8C$\frac{\underline{\;����\;}}{\;}$3Na2S+4CO2��+4CO����
�ʴ�Ϊ��3Na2SO4+8C$\frac{\underline{\;����\;}}{\;}$3Na2S+4CO2��+4CO����
��2�����������в���ϡ��Һ������ˮ���ã�������Һ��������ˮ���Լ��ԣ�ˮ����������ȷ�Ӧ�����ȴٽ�ˮ����У�ϡ����Һ��������ˮ������ã�
�ʴ�Ϊ����ˮ��ٽ�Na2Sˮ�⣬��ϡ��Һ������Na2Sˮ�⣻
��3������ͼ�������߷�������ȥ�������PH��x��ȡֵ��x=12 pH����9��10֮��ʱ����ȥ������ӽ�100%��
�ʴ�Ϊ��x=12�� pH����9��10֮�䣻
��4��ȡ���ƾ��壨������NaOH�����뵽����ͭ��Һ�У���ֽ��裬����Ӧ������Һ��pH=4��c��OH-��=10-10mol/L��
����ʱCuS��Cu��OH��2��Ksp�ֱ�Ϊ8.8��10-36��2.2��10-20��
����������ͭ���ܶȻ��ɵã�Ksp=c��Cu2+����c2��OH-��=2.2��10-20����ã�c��Cu2+��=$\frac{2.2��1{0}^{-20}}{��1{0}^{-10}��^{2}}$mol/L=2.2mol/L��
������ͭ���ܶȻ��ɵã�Ksp=c��Cu2+��c��S2-��=8.8��10-36��
���ʱ��Һ��c�� S2-��=$\frac{8.8��1{0}^{-36}}{2.2}$mol/L=4.0��10-36mol/L��
�ʴ�Ϊ��4.0��10-36mol/L��
���� ���⿼���������Ʊ������ԭ������Ӧ�õ�֪ʶ����Ŀ�Ѷ��еȣ������漰�����Ʊ�ԭ������ѧ����ʽ��д���������ԭ�����缫��Ӧʽ����д���ܶȻ������ļ���ȣ�������ؿ���ѧ���ķ������������������Ӧ����ѧ֪ʶ����������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���ӱ� | B�� | ����1mol C | C�� | ������1mol | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��d��f֮�ȿ���Ϊ16��1��3 | |
| B�� | һ����a=2e��b=e | |
| C�� | ��n��KClO����n��KClO3��=1��1����a��b��c��d��e��f����Ϊ8��4��6��1��4��1 | |
| D�� | �����÷���ʽ��д���������뷴Ӧ��������һ����Cl2-2e-=2Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ֱ�������۹۲����ʵ���ɫ��״̬ | |
| B�� | ��ҩƷ����ζ | |
| C�� | Ʒ�����ʵ�ζ�� | |
| D�� | �����������й۲� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
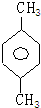 ����һ�ȴ���Ľṹ��ʽ��
����һ�ȴ���Ľṹ��ʽ��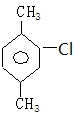 ������һ�ȴ�������������
������һ�ȴ�������������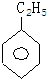 ��������ṹ��ʽ��
��������ṹ��ʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/��g•L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com