
| A. | 1:4 | B. | 1:3 | C. | 1:1 | D. | 4:1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
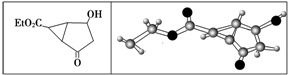
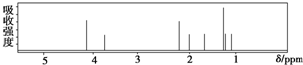
| A. | 该有机物分子中不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH2CH3 | |
| D. | 该有机物可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
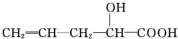 在不同条件下至少可能发生不同类型的反应:①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤酯化反应,⑥加聚反应,其中由于其分子结构中含有-OH,可能发生的反应有( )
在不同条件下至少可能发生不同类型的反应:①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤酯化反应,⑥加聚反应,其中由于其分子结构中含有-OH,可能发生的反应有( )| A. | ②④ | B. | ①③④⑤⑥ | C. | ②③④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第IIIA的铊(Tl)既能与盐酸作用产生氢气,又能跟NaOH溶液反应放出氢气 | |
| B. | 第VIIA的砹(At)为有色固体,易溶于四氯化碳,但难溶于水 | |
| C. | 第IIA的锶的硫酸盐(SrSO4)是易溶于水的白色固体 | |
| D. | 第VIA的硒的氢化物(H2Se)是无色、有毒,比H2S稳定的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO与O2在反应生成NO2 | B. | 硝酸工厂用NH3氧化制NO | ||
| C. | 雷雨时空气中的N2转化为NO | D. | 由NH3制碳酸氢铵和硫酸铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
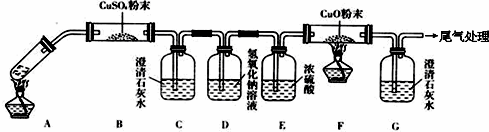
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 实验室用装置①制取氨气 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③可用于制备氢氧化亚铁并观察其颜色 | |
| D. | 装置④b口进气可收集CO2等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、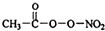 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com