
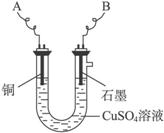
(1)实验中测定在标准状况下放出的氧气的体积V L(氧元素的相对原子质量为16),A、B分别连接直流电源的_______________和______________ (填正极或负极)。
(2)电解开始一段时间后,在U形管中可观察到的现象有______________;电解的离子方程式为______________。
(3)实验中还须测定的数据是(填写序号)____________________________。
①A极的质量增重m g
②B极的质量增重m g
(4)铜的相对原子质量为(用含有m、V的计算式表示)______________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对分子质量.
某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对分子质量.
| ||
| ||
| 11.2m |
| M |
| 11.2m |
| M |
查看答案和解析>>
科目:高中化学 来源: 题型:
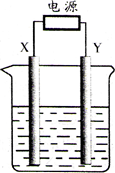 某化学兴趣小组用图示装置进行电解原理的实验探究.
某化学兴趣小组用图示装置进行电解原理的实验探究.查看答案和解析>>
科目:高中化学 来源: 题型:
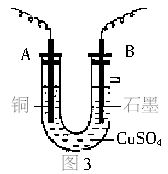
某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量(如图3)。
(1)若实验中测得在标准状况下放出的氧气的体积为VL,则A、B分别连接直流电源的________和__________(填“正极”或“负极”)。
(2)电解开始一段时间后,在U形管中可观察到的现象有
___________, ___________。电解的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年黑龙江省双鸭山市高三上学期第二次月考化学试卷(解析版) 题型:填空题
某化学兴趣小组用下图装置电解CuSO4溶液,测定铜的相对分子质量。

(1)若实验中测定在标准状况下放出的氧气的体积VL,A连接直流电源的__________ (填“正极”或“负极”)。
(2)电解开始一段时间后,在U形管中可观察到的现象-____________________________。
电解的离子方程式为 。
(3)实验中还需测定的数据是_______________(填写序号)。
①A极的质量增重m g ②B极的质量增重m g
(4)下列实验操作中必要的是____________(填字母)。
A.称量电解前电极的质量
B.电解后,电极在烘干称重前,必须用蒸馏水冲洗
C.刮下电解过程中电极上析出的铜,并清洗、称重
D.电极在烘干称重的操作中必须按“烘干—称重一再烘干一再称重”进行
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为:_______________________(用含有m、V的计算式表示)。
(6)如果用碱性(KOH为电解质)甲醇燃料电池作为电源进行实验,放电时负极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com