
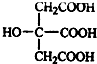 .
. 分析 (1)化合物A中C、H、O三种元素的质量分数分别为37.5%、4.2%和58.3%,则N(C):N(H):N(O)=$\frac{37.5%}{12}$:$\frac{4.2%}{1}$:$\frac{58.3%}{16}$=6:8:7,设A的化学式为(C6H8O7)x,0.01molA在空气中充分燃烧需消耗氧气1.01L,则0.01x×(6+$\frac{8}{4}$-$\frac{7}{2}$)×22.4=1.01,x=1,A的化学式为C6H8O7;
(2)A不能发生银镜反应,说明A中不含醛基,1molA与足量的碳酸氢钠溶液反应可以放出3mol二氧化碳,说明A中含有3个羧基,在浓硫酸催化下,A与乙酸发生酯化反应,说明A中含有羟基;核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境,A的结构简式为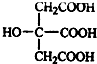 .
.
解答 解:(1)化合物A中C、H、O三种元素的质量分数分别为37.5%、4.2%和58.3%,则N(C):N(H):N(O)=$\frac{37.5%}{12}$:$\frac{4.2%}{1}$:$\frac{58.3%}{16}$=6:8:7,设A的化学式为(C6H8O7)x,0.01molA在空气中充分燃烧需消耗氧气1.01L,则0.01x×(6+$\frac{8}{4}$-$\frac{7}{2}$)×22.4=1.01,x=1,A的化学式为C6H8O7,
故答案为:C6H8O7;
(2)A中不饱和度=$\frac{6×2+2-8}{2}$=3,说明A中含有三个双键,A中不含醛基,1molA与足量的碳酸氢钠溶液反应可以放出3mol二氧化碳,说明A中含有3个羧基,在浓硫酸催化下,A与乙酸发生酯化反应,说明A中含有羟基;核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境,结合其分子式知,A的结构简式为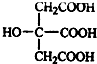 ,故答案为:
,故答案为: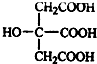 .
.
点评 本题考查了有机物的推断,为高频考点,侧重于学生的分析能力和计算能力的考查,根据有机物的性质确定存在的官能团,再结合分子确定其结构简式,题目难度中等.


科目:高中化学 来源: 题型:推断题
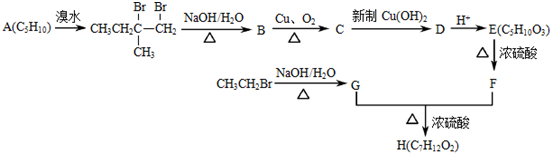
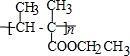 .
.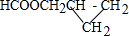 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
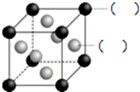 A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为紫红色固体,可通过“湿法冶金”而得.请回答下列问题:
A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为紫红色固体,可通过“湿法冶金”而得.请回答下列问题: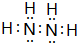 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| H2(g) | Br2(g) | HBr(g) |
| 436kJ | akJ | 369kJ |
| A. | 200 | B. | 230 | C. | 260 | D. | 404 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 被还原的硝酸的物质的量是0.12mol | |
| C. | 得到5.08g沉淀时,加入NaOH溶液的体积是700mL | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 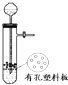 图所示装置用于Cu和浓H2SO4反应制取少量的SO2气体 图所示装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. | 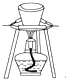 图所示装置用于除去碳酸氢钠固体中的少量碳酸钠 图所示装置用于除去碳酸氢钠固体中的少量碳酸钠 | |
| C. | 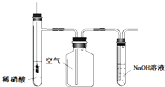 图所示装置用于制备并收集NO气体 图所示装置用于制备并收集NO气体 | |
| D. | 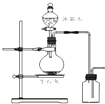 图所示装置制取并收集氨气 图所示装置制取并收集氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
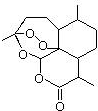
 ,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)
,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)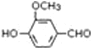 )可用于合成青蒿素,合成天然香草醛的反应如图:
)可用于合成青蒿素,合成天然香草醛的反应如图: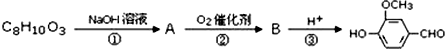
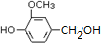 .
.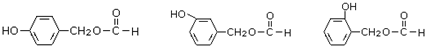 .
.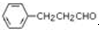 是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).
是合成青蒿素的中间原料之一,写出由苯甲醛和氯乙烷为原料,制备苄基乙醛的合成路线流程图(无机试剂任用).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com