
【题目】已知烯烃在酸性KMnO4溶液中双键断裂形式为: 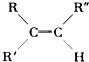
![]()
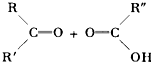 现有二烯烃C10H18与酸性KMnO4溶液作用后可得到三种有机物:(CH3)2CO、CH3COOH、CH3CO(CH2)2﹣COOH,由此推断此二烯可能的结构简式为( )
现有二烯烃C10H18与酸性KMnO4溶液作用后可得到三种有机物:(CH3)2CO、CH3COOH、CH3CO(CH2)2﹣COOH,由此推断此二烯可能的结构简式为( )
A.(CH3)2C═C(CH3)CH2CH2CH═CH CH2CH3
B.(CH3)2C═CHCH2CH2C(CH3)═CHCH3
C.CH3CH═C(CH3)CH2CH2CH2C(CH3)═CH2
D.CH3CH═C(CH3)CH2CH2CH2CH═CHCH3
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.8kJ的热量(相当于25℃、101kPa下测得的热量). ①反应的热化学方程式为 .
②又已知H2O(l)═H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是kJ.
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 .
(2)已知热化学方程式:①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣25kJmol﹣1②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=﹣47kJmol﹣1
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=19kJmol﹣1
写出FeO(s)被CO还原生成Fe和CO2的热化学方程式: .
(3)已知反应2HI(g)═H2(g)+I2(g)的△H=+11kJmol﹣1 , 1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436KJ、151KJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为kJ.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题:
(1)图中所示反应是(填“吸热”或“放热”)反应,该反应的△H=(用含E1、E2的代数式表示).
(2)下列4个反应中符合示意图描述的反应的是 (填代号).
A.水蒸气与炭反应
B.用水稀释氢氧化钠溶液
C.铝粉与Fe2O3反应
D.灼热的碳与CO2反应
(3)已知热化学方程式:H2(g)+ ![]() O2 (g)=H2O(g)△H=﹣241.8kJ/mol.该反应的活化能为167.2kJ/mo1,则其逆反应的活化能为 .
O2 (g)=H2O(g)△H=﹣241.8kJ/mol.该反应的活化能为167.2kJ/mo1,则其逆反应的活化能为 .
(4)以甲烷为原料制取氢气是工业上常用的制氢方法.已知:
CH4 (g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2 (g)△H=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1mol H2O分子中含有6.02×1023个微粒 B. 44gCO2中含有1.204×1024个O原子
C. NH3的摩尔质量为17 D. 44.8L CH4含有2mol C原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,叫做反应热.由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等.
(1)下列△H表示物质标准燃烧热的是 ;表示中和反应反应热的是 .(填“△H1”、“△H2”、“△H3”等)
A.2H2(g)+O2(g)═2H2O(l)△H1B.C(s)+![]() O2(g)═CO(g)△H2=﹣Q1kJmol﹣1
O2(g)═CO(g)△H2=﹣Q1kJmol﹣1
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3D.C(s)+O2(g)═CO2(g)△H4=﹣Q2kJmol﹣1
E.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H5
(2)2.00g C2H2气体完全燃烧生成液态水和CO2气体,放出99.6kJ的热量,写出该反应的热化学方程式: .
(3)根据题(1)中B、D判断1molCO(g)完全燃烧的△H= .
(4)反应E的△H6可以用如图所示的装置进行测量.实验中直接测定的数据是 ;从实验装置上看,图中尚缺少的一种玻璃用品是 ;大烧杯上如不盖硬纸板,求得的中和反应的反应热的数值 (填“偏大”“偏小”或“无影响”).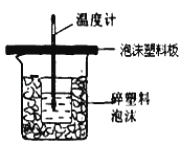
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
A.若增大压强,则物质Y的转化率减小
B.将容器体积变为5 L,Z的平衡浓度变为原来的2倍
C.Y浓度变化表示的反应速率为0.0005 mol/(Ls )
D.若升高温度,X的体积分数增大,则该反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类说法正确的是( )
A. 纯碱、液态氧、碘酒、稀盐酸依次是盐、单质、混合物、电解质
B. 干冰、生石灰、硫酸、碳酸氢铵依次是单质、氧化物、酸、盐
C. 氯化氢、氨气、水银、草木灰依次是电解质、非电解质、单质、混合物
D. 冰水、空气、泥水依次是溶液、胶体、浊液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com