
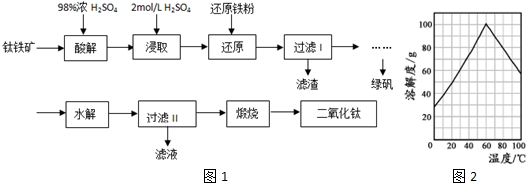
分析 钛铁矿的主要成分为FeTiO3,在343K-353K条件下钛铁矿和浓硫酸混合,发生的反应有FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O、Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,得到固体熔块,然后用水浸取,浸取液中含有Fe3+,Fe3+能和Fe反应生成Fe2+,然后过滤,得到的晶体X成分为硫酸亚铁,TiOSO4能发生水解反应生成H2TiO3和H2SO4,最后高温煅烧得到TiO2,据此分解解题.
(1)根据:FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O分析是复分解反应,生成TiOSO4的反应也为复分解反应;
(2)根据:FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O反应计算,消耗浓硫酸最多;
(3)提高浸出率可通过增大接触面积和时间上等因素考虑;
(4)根据2Fe3++Fe=3Fe2+可知,加“还原铁粉”的目的是将溶液里的Fe3+还原为Fe2+;
(5)请根据FeSO4溶解度曲线,从过虑I中滤液获得副产品绿矾(FeSO4•7H2O)的具体操作为加热浓缩到60℃饱和溶液,冷却至0℃结晶、过滤,少量冰水洗涤、低温干燥;
(6)水解是吸热过程,将滤液加热至90℃作用是促进TiOSO4和Ti2(SO4)3的水解;沉淀用2mol/LH2SO4溶液洗涤而不是用水洗涤的原因防止Fe2+水解而造成产物不纯.
解答 解:(1)根据:FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O分析是复分解反应,得出生成TiOSO4的化学方程式为2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O,
故答案为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O;
(2)设消耗浓硫酸xmL
FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O
152 3×98
5g 1.84g/mL×xmL×98%
x=6.13mL.
故答案为:B
(3)提高浸出率可通过增大接触面积和时间上等因素考虑,粉碎矿石、适量处长浸取时间等,故答案为:粉碎矿石、适量处长浸取时间;
(4)根据2Fe3++Fe=3Fe2+可知,加“还原铁粉”的目的是将溶液里的Fe3+还原为Fe2+,故答案为:将溶液中的Fe3+还原成Fe2+
(5)请根据FeSO4溶解度曲线,从过虑I中滤液获得副产品绿矾(FeSO4•7H2O)的具体操作为加热浓缩到60℃饱和溶液,冷却至0℃结晶、过滤,少量冰水洗涤、低温干燥,故答案为:加热浓缩到60℃饱和溶液,冷却至0℃结晶、过滤,少量冰水洗涤、低温干燥;
(6)水解是吸热过程,将滤液加热至90℃作用是促进TiOSO4和Ti2(SO4)3的水解;沉淀用2mol/LH2SO4溶液洗涤而不是用水洗涤的原因防止Fe2+水解而造成产物不纯,故答案为:促进TiOSO4和Ti2(SO4)3的水解 防止Fe2+水解而造成产物不纯.
点评 以物质分离和提纯和制备为载体考查化学工艺流程,涉及化学方程式配平、溶解度、结晶、沉淀的洗涤和溶液的配制、盐的水解等.明确化学原理及物质性质是解本题关键,本题较难.


科目:高中化学 来源: 题型:选择题
| A. | “可燃冰”给我们提供了水可以变油的证据 | |
| B. | CH4•(H2O)n属于氧化物 | |
| C. | “可燃冰”是燃烧值高,没有污染的新能源 | |
| D. | 开采不当可造成比二氧化碳更严重的温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
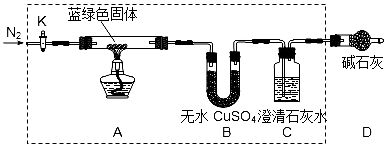
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
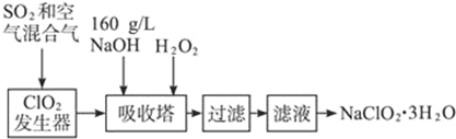
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 物质 | 熔点 | 沸点 | 溶解度 |
| 乙酰苯胺 | 114.3℃ | 305℃ | 微溶于冷水、易溶于热水 |
| 苯胺 | -6℃ | 184.4℃ | 微溶于水 |
| 醋酸 | 16.6℃ | 118℃ | 易溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{118}^{175}$X | B. | ${\;}_{175}^{118}$X | C. | ${\;}_{118}^{293}$X | D. | ${\;}_{293}^{118}$X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
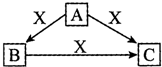 A、B、C、X均为中学化学常见的物质,一定条件下,它们有如下转化关系(部分产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见的物质,一定条件下,它们有如下转化关系(部分产物已略去),下列说法错误的是( )| A. | 若X为Cl2,则C可能为FeCl3 | |
| B. | 若X为KOH溶液,则A可能为AlCl3溶液 | |
| C. | 若X为Fe,则A可能为HNO3 | |
| D. | 若A、B、C均为焰色反应呈黄色的化合物,则X可能为CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com