
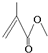
 ,它的分子式为C5H8O2,存在的官能团有碳碳双键和酯基,该物质能发生的反应类型有加成反应、氧化反应、水解反应.
,它的分子式为C5H8O2,存在的官能团有碳碳双键和酯基,该物质能发生的反应类型有加成反应、氧化反应、水解反应.分析 (1)根据键线式的特点以线示键,每个折点和线端点处表示有一个碳原子,并以氢原子补足四键,C、H原子不表示出来,写化学式;常见的官能团有:碳碳双键、碳碳三键、羟基、羧基、酯基等;
(2)乙醇的分子式是:C2H6O,结构简式是:CH3CH2OH或C2H5OH、乙醇分子中官能团是羟基(-OH),制备乙醇需引入羟基,根据备选物质合成.
解答 解:(1)根据键线式的书写特点,图 ,每个折点和线端点处表示有一个碳原子,并以氢原子补足四键,它的分子式为C5H8O2,官能团为碳碳双键和酯基,
,每个折点和线端点处表示有一个碳原子,并以氢原子补足四键,它的分子式为C5H8O2,官能团为碳碳双键和酯基,
故答案为:C5H8O2;碳碳双键和酯基;加成反应、氧化反应、水解反应;
(2)乙醇的分子式是:C2H6O,结构简式是:CH3CH2OH或C2H5OH、乙醇分子中官能团是羟基(-OH),制备乙醇需引入羟基,乙烯含有碳碳双键,可由双键的水化引入羟基,反应为:CH2=CH2+H2O$\stackrel{一定条件}{→}$C2H5OH,也可由卤代烃在碱性条件下的水解制取,反应为:C2H5Br+NaOH$\stackrel{△}{→}$C2H5OH+NaBr+H2O,醛基的氢化也能引入醇羟基,反应为:CH3CHO+H2$→_{△}^{催化剂}$C2H5OH,也可为酯的水解,乙酸乙酯在酸性条件下水解生成乙酸和乙醇,化学反应方程式为:CH3COOC2H5+H2O$?_{△}^{酸}$CH3COOH+CH3CH2OH,
故答案为:CH2=CH2+H2O$\stackrel{一定条件}{→}$C2H5OH;C2H5Br+NaOH$\stackrel{△}{→}$C2H5OH+NaBr+H2O;CH3CHO+H2$→_{△}^{催化剂}$C2H5OH,CH3COOC2H5+H2O$?_{△}^{酸}$CH3COOH+CH3CH2OH.
点评 本题主要考查了键线式的特点、有机物的合成,抓住键线式特点即可写出其分子式.,明确常见的烃的衍生物的官能团类型及具有的化学性质是解答制备乙醇的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体具有吸附性,可做净水剂 | |
| B. | 该胶体的分散系的分散质粒子的直径大小 是10-9nm-10-7nm之间 | |
| C. | 可用丁达尔效应鉴别氢氧化铁胶体和水 | |
| D. | 可用渗析的方法分离FeCl3溶液和Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=+57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$ O2 (g)=8CO2 (g)+9H2O(g)△H=-5518kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)=16CO2 (g)+18H2O(1)△H=-11036kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
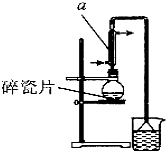 醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备 1-溴丁烷的反应和实验装置如下:
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备 1-溴丁烷的反应和实验装置如下:| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | |
| 正丁醇 | -89.53 | 117.25 | 0.81 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)×(10-4mol•L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| C(CO)×(10-3mol•L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
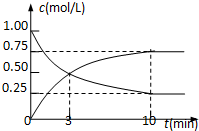 为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.目前,工业上常用CO2来生产燃料甲醇.现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.
为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.目前,工业上常用CO2来生产燃料甲醇.现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com