
甲酸的下列性质中可以证明它是弱电解质的是( )
A. 1 mol·L-1的甲酸溶液的c(H+)约为0.01 mol·L-1
B. 甲酸与水以任意比例互溶
C. 10 mL 1 mol·L-1甲酸恰好与10 mL 1 mol·L-1NaOH溶液完全反应
D. 甲酸溶液的导电性比盐酸溶液的弱
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
常温下,某学生从一种强酸性的未知无色溶液中检出Ag+,他还想通过实验检验溶液中是否含有大量的Cl-、CO32-、Cu2+、Fe3+、K+等。你认为其中
是需要检验的,而 是不需要检验的。其原因是  。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为 ,它可以发生反应的类型有:①加成 ②消去
,它可以发生反应的类型有:①加成 ②消去
③水解 ④酯化 ⑤氧化 ⑥加聚 ( )
A.①②③④ B.①②④⑤ C.①②⑤⑥ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质:①12C和14C ②CH3(CH2)5CH3和CH3CH=CHCH(CH3)C2H5
③CH3CH2CH2CH3和(CH3)2CHCH3 ④H2、D2、T2 ⑤癸烷和十六烷
|
|
|
⑥O2和O3
A.互为同位素的是(填序号,下同) ;B.互为同系物的是 ;
C.互为同分异构体的是 ; D.为同一种物质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将pH=3的盐酸和10-3 mol·L-1的氨水等体积混和后,溶液中离子浓度关系正确的是( )
A.[NH4+]>[Cl-]>[H+]>[OH-] B.[NH4+]>[Cl-]>[OH-]>[H+]
C.[Cl-]>[NH4+]>[H+]>[OH-] D.[Cl-]>[NH4+]>[OH-]> [H+]
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温时,一固定容积的容器内发生如下反应:2NH3 (g) 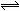 N2 (g)+3H2 (g),达平衡后,再向容器内通入一定量的NH3(g),重新达到平衡后,与第一次平衡时相比,NH3的体积分数( )
N2 (g)+3H2 (g),达平衡后,再向容器内通入一定量的NH3(g),重新达到平衡后,与第一次平衡时相比,NH3的体积分数( )
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
“嫦娥一号”的登月成功,实现了中国人“奔月”的梦想。
⑴ 2H2(g)+O2(g)=2H2O(l); H=-571.6kJ·mol-1
H=-571.6kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
C8H18(l)+12.5O2(g)=8CO2(g)+9H2O(l); H=-5518 kJ·mol-1
H=-5518 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l)  H =-890kJ·mol-1
H =-890kJ·mol-1
相同质量的H2 、C、 C8H18 、CH4完全燃烧时,放出热量最多的是 。
⑵ 氢气、氧气不仅燃烧能放出热量,二者形成的原电池还能提供电能。“嫦娥一号”绕月飞行部分使用的是氢氧燃料电池,电解质溶液为KOH溶液,其电极反应式为:
负极 ;正极 ;
⑶若用氢氧燃料电池电解100mL由NaCl 和CuSO4组成的混合溶液,其中
[Na+]=3[Cu2+]=0.3mol·L-1,用石墨作电极,通电一段时间后,在阴极收集到0.112L H2(标况).
试计算:
①阴极析出Cu mol。阳极析出气体为 (填化学式)。
②若所得溶液仍然为100mL,则此时溶液的pH值为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaCl2溶液中通入下列气体后,溶液中一定会出现白色沉淀的是( )
A. SO2 B. 先通NO2 ,后通SO2 C. 先通SO2,后通H2S D. NH3,CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学原理表述正确的是
A.氢硫酸溶液加水稀释,电离程度增大,H+浓度增大
B.同体积同pH的盐酸和醋酸与足量的锌反应,醋酸的反应速率快,生成H2的
物质的量多
C.NaHCO3溶液不显中性的原因:HCO3-+H2O ≒ CO32-+H3O+
D.Na2CO3溶液中满足:2c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com