
| A、向加有酚酞的NaOH溶液中通入氯气,溶液立即褪色 |
| B、向加有酚酞的水中投入少量Na2O2粉末,溶液先变红,后褪色 |
| C、显红色的酚酞溶液中通入SO2后,红色褪去 |
| D、向溶有KMnO4的酸性溶液中通入SO2后,溶液紫红色褪去 |


科目:高中化学 来源: 题型:
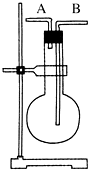 ①H2②Cl2③NH3④O2⑤CH4⑥NO ⑦NO2⑧SO2⑨HCl.
①H2②Cl2③NH3④O2⑤CH4⑥NO ⑦NO2⑧SO2⑨HCl.| A、在烧瓶中充满水,由B进气收集④⑥ |
| B、在烧瓶中充满水,由A进气收集①③⑤⑥⑦ |
| C、烧瓶是干燥的,由B进气收集②④⑥⑦⑧⑨ |
| D、烧瓶是干燥的,由A进气收集①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Al3+、CO32-、Cl- |
| B、Na+、H+、SO42-、SiO32- |
| C、H+、Mg2+、SO42-、I- |
| D、H+、Fe2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释溶液,水解平衡常数增大 | ||||||
B、升高温度,
| ||||||
| C、通入CO2,平衡右移动 | ||||||
| D、加入NaOH(s),溶液pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水玻璃和亚硫酸钠长期暴露在空气中均易变质 |
| B、浓硝酸和氯水均用棕色试剂瓶保存 |
| C、NaCl固体中混有NH4Cl或I2,均可用加热法除去 |
| D、浓硫酸和浓盐酸长期暴露在空气中浓度均降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B、Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
| D、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的电离方程式:H2O═H++OH- |
| B、升高温度,水的电离程度增大 |
| C、在NaOH溶液中没有H+,在HCl溶液中没有OH- |
| D、纯水中c(H+)=10-7 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
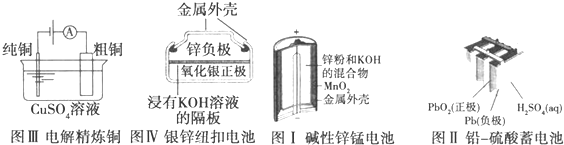
| A、图Ⅰ所示电池中,MnO2作催化剂 |
| B、图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C、图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 |
| D、图Ⅳ所示电池中,Ag2O作氧化剂,在电池工作过程中被还原为Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了提高生活用水的卫生标准,自来水厂常同时使用Cl2和FeSO4?7H2O进行消毒、净化,以改善水质 |
| B、铝表面有一层致密的氧化薄膜,故铝制容器可用来腌制咸菜等 |
C、 从分类的角度看,混合物、分散系、胶体的从属关系如图所示: |
| D、借助扫描隧道显微镜,应用STM技术可实现对原子或分子的操纵 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com