

分析 由流程可知,设备①中含有苯酚和工业废水,可经萃取、分液得到苯酚的苯溶液混合物,进入设备②,设备②加入氢氧化钠溶液,可得到苯酚钠,在设备③中通入二氧化碳可得到苯酚,发生C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,设备④中的主要物质为NaHCO3,在溶液中加入氧化钙,可生成氢氧化钠和碳酸钙沉淀,
(1)工业废水与苯进入设备①得到苯酚、苯的溶液与可以排放的无酚工业废水,说明在设备①中进行的是萃取;
(2)盛有苯酚、苯溶液的设备②中注入氢氧化钠溶液,此时,具有酸性的苯酚跟氢氧化钠发生反应,生成苯酚钠和水,由设备②进入设备③的物质A是C6H5ONa,在设备②中的液体分为两层,上层是苯层,下层是苯酚钠的水溶液,上层的苯通过管道送回设备①中继续萃取工业废水中的苯酚,循环使用,下层的苯酚钠溶液进入设备③;在盛有苯酚钠溶液的设备③中,通入过量的二氧化碳气,发生化学反应,生成苯酚和碳酸氢钠;
(3)苯酚钠溶液通入过量二氧化碳,生成苯酚和碳酸氢钠;
(4)物质B为碳酸氢钠溶液,碳酸氢钠与氧化钙反应生成碳酸钙沉淀和强氧化钠,然后通过过滤可以分离出碳酸钙和氢氧化钠;
(5)根据生产流程图中的物质,找出反应物与生成物,然后分析生成物中的物质被用作反应物的即为可循环利用的物质.
解答 解:由流程可知,设备①中含有苯和工业废水,可经萃取、分液得到苯酚的苯溶液混合物,进入设备②,设备②加入氢氧化钠溶液,可得到苯酚钠,在设备③中通入二氧化碳可得到苯酚,发生C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,设备④中的主要物质为NaHCO3,在溶液中加入氧化钙,可生成氢氧化钠和碳酸钙沉淀,
(1)工业废水与苯进入设备①得到苯酚、苯的溶液与可以排放的无酚工业废水,说明在设备①中进行的是萃取,利用苯与苯酚相似的结构互溶与水不溶,将苯酚从工业废水里提取出来,用分液的方法将下层的工业废水放出排放,上层的苯酚、苯混合液进入设备②;萃取、分液必须用到的仪器名称叫分液漏斗,
故答案为:分液;分液漏斗;
(2)盛有苯酚、苯溶液的设备②中注入氢氧化钠溶液,此时,具有酸性的苯酚跟氢氧化钠发生反应,生成苯酚钠和水,由设备②进入设备③的物质A是C6H5ONa,在设备②中的液体分为两层,上层是苯层,下层是苯酚钠的水溶液,上层的苯通过管道送回设备①中继续萃取工业废水中的苯酚,循环使用,下层的苯酚钠溶液进入设备③,在盛有苯酚钠溶液的设备Ⅲ中,通入过量的二氧化碳气,发生化学反应,生成苯酚和碳酸氢钠,
故答案为:C6H5ONa;NaHCO3;
(3)依据碳酸性比苯酚的酸性强,弱酸盐与“强”酸发生的复分解反应,二氧化碳和苯酚钠反应生成苯酚,反应的方程式为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,
故答案为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;
(4)盛有碳酸氢钠溶液的设备④中,加入生石灰,生石灰与碳酸氢钠溶液里的水反应生成氢氧化钙,熟石灰和与碳酸氢钠发生复分解反应,生成碳酸钙沉淀、水、氢氧化钠,有关反应方程式为:CaO+H2O=Ca(OH)2,Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O,所以产物为CaCO3、NaOH和水,可通过过滤操作分离出碳酸钙和氢氧化钠,
故答案为:CaCO3;NaOH;过滤;
(5)设备④应是石灰窑,CaCO3高温分解所得的产品是氧化钙和二氧化碳,所得二氧化碳通入设备③,反应所得氧化钙进入设备④.在含苯酚工业废水提取苯酚的工艺流程中,苯、氧化钙、CO2、和NaOH理论上应当没有消耗,它们均可以循环使用,
故答案为:CO2;NaOH.
点评 本题考查了化学实验基本操作方法的综合应用,题目难度中等,明确工艺流程及反应原理为解答关键,注意掌握化学实验基本操作方法,试题侧重考查学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | CDEAB | B. | ECDAB | C. | BAEDC | D. | BADCE |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥⑧ | B. | ②④ | C. | ①②⑤ | D. | ①④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸在浓硫酸作用下制硝基苯 | |
| C. | 乙醇与乙酸的酯化反应 | |
| D. | 一定条件下苯与氢气反应制环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧 | B. | NaOH溶液 | ||
| C. | 溴的四氯化碳溶液 | D. | 酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
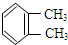 与
与 是同一物质;
是同一物质;| A. | ①②③④ | B. | ①③④ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷.卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如图所示.该结构中氯原子有两种不同位置.
白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷.卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如图所示.该结构中氯原子有两种不同位置.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com