
分析 pH=12的氢氧化钡溶液的物质的量浓度是溶液中氢氧根离子浓度的一半;稀释前后,溶液中溶质的物质的量不变化,体积变化,0.01mol/LNaOH溶液中水电离出的c(OH-)=c(H+),根据Kw=c(OH-)•c(H+)来计算即可.
解答 解:pH=12的氢氧化钡溶液中c(OH-)=0.01mol/L,氢氧化钡溶液的物质的量浓度是溶液中氢氧根离子浓度的一半,即pH=12的氢氧化钡溶液的物质的量浓度为 0.005mol/L,稀释100倍后,溶液中溶质的物质的量不变化,体积变为原来的100倍,所以氢氧根离子浓度是原来的0.01倍,即此时pH=10,某温度下,纯水电离出c(H+)=2×10-7mol/L,则该温度下Kw=c(OH-)•c(H+)=4×10-14,该温度下0.01mol/LNaOH溶液中水电离出的c(OH-)=$\frac{4×1{0}^{-14}}{0.01}$mol/L=4×10-12mol/L,
故答案为:0.005mol/L;10;4×10-12mol/L.
点评 本题考查了pH的简单计算,注意无论酸还是碱溶液,水电离出来的c(OH-)=c(H+),为易错点.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CuCl2(无水CuSO4) | B. | NaOH(H2O) | C. | NaCl(HCl气体) | D. | CuSO4(Cu(OH)2固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
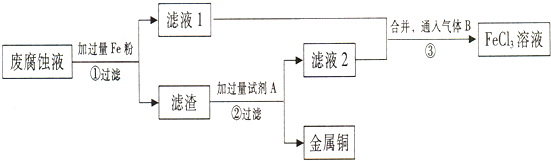
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
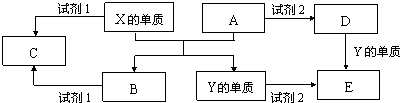
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com