
下列化学方程式或离子方程式中,书写正确的是( )
A.氢氧化铜溶于醋酸溶液中:Cu(OH)2+2H+=Cu2++2H2O
B.乙醛的银镜反应:CH3CHO+Ag(NH3)2OH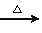 CH3COONH4+NH3+Ag↓+H2O
CH3COONH4+NH3+Ag↓+H2O
C.苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O C6H5OH+HCO3-
C6H5OH+HCO3-
D.丙烯聚合:
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:2015-2016学年湖南师大附中高一下期中化学试卷(解析版) 题型:选择题
下列物质中,既含有共价键又含有离子键的是
A.HCl B.Na2S C.MgCl2 D.NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北武汉华中师大一附高一下期中化学试卷(解析版) 题型:选择题
下列结论正确的是
A.某元素的一种核素的核内质子数为m,中子数为n,由此一定能确定该元素的近似相对原子质量为m+n
B.短周期元素X、Y、Z,X的阳离子与Y的阴离子具有相同的电子层结构,Z的阴离子的还原性大于等电荷数Y的阴离子的还原性,那么原子序数大小是Z>X>Y
C.第118元素在元素周期表中的位置是第七周期VIA族
D.碱金属单质的熔沸点和卤素单质的熔沸点都是随核电荷数的递增而升高
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:填空题
A、B、C、D、E是前四周期原子序数依次增大的五种元素。A元素原子的核外电子数等于其电子层数,B元素基态原子有三个能级且各能级电子数相同, A与D可形成两种常见液态化合物G、H,其原子数之比分别为1:1和2:1。E元素原子的K、L层电子数之和等于其M、N层电子数之和。请回答下列各题(涉及元素请用相应化学符号表示):
(1) B、C、D三种元素中电负性最大的元素其基态原子的电子排布图为 。
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用 形象化描述。在B的基态原子中,核外存在 对自旋相反的电子。
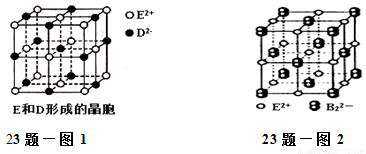
(3)由E和D形成的晶胞如图1所示,晶体中E2+周围等距且最近的E2+有________个;ED的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色反应,其原因是 。E和B可形成的晶体的晶胞结构与NaCl晶体的相似(如图2所示),但该晶体中含有的哑铃形B22-的存在,使晶胞沿一个方向拉长。晶体中E2+的配位数为______。该化合物的电子式为 。
(4)用高能射线照射液态H时,一个H分子能释放出一个电子,同时产生一种阳离子。
①释放出来的电子可以被若干H分子形成的“网”捕获,你认为H分子间能形成“网”的原因是 。
②由H分子释放出一个电子时产生的一种阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式 ;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:选择题
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示,关于咖啡鞣酸的下列叙述正确
的是 ( )

A.分子式为C16H20O9
B.1mol咖啡鞣酸水解时可消耗8mol NaOH
C.与苯环直接相连的原子都在同一平面上
D.能发生取代反应和加成反应,但不能消去反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:选择题
如图是蓝色晶体MxFey(CN)6中阴离子的最小结构单元(图中是该晶体晶胞的八分之一)下列说法正确的是( )
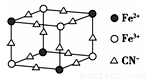
A.该晶体属于离子晶体,M呈+2价
B.该晶体属于分子晶体,化学式为MFe2(CN)6
C.该晶体中与每个Fe3+距离相等且最近的CN-为12个
D.该晶体的一个晶胞中含有的M+的个数为4个
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三5月月考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】硼和氮元素在化学中有很重要的地位,回答下列问题:
(1)基态硼原子核外电子有____ ____种不同的运动状态,基态氮原子的价层电子排布图为_________________。预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2]。(CH3)2NNH2中N原子的杂化方式为_________。
(2)化合物H3BNH3是一种潜在的储氢材料,可利用化合物B3N3H6通过如下反应制得:3CH4+2B3N3H6+ 6H2O=3CO2+6H3BNH3
①H3BNH3分子中是否存在配位键_______________(填“是”或“否”),B、C、N、O的第一电离能由小到大的顺序为___________________。
②与B3N3H6互为等电子体的分子是_____________(填一个即可),B3N3H6为非极性分子,根据等电子原理写出B3N3H6的结构式____________________________。
(3)“嫦娥五号”探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质,回答下列问题:
①SeO3分子的立体构型为_____________。
②金属铜投入氨水或H2O2溶液中均无明显现象,但投入氨水与H2O2的混合溶液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子反应方程式为 。
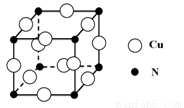
③某种铜合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子间的距离为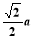 pm,则该晶体的密度为_________________(用含a的代数式表示,设NA为阿
pm,则该晶体的密度为_________________(用含a的代数式表示,设NA为阿
伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2 。用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·x H2O的化学方程式为
(2)玻璃棒有多种用途,下列实验操作中玻璃棒的作用完全相同的是 (填字母)
①测定醋酸钠溶液的pH ②加热食盐溶液制备NaCl晶体
③配制0.1mol/L的硫酸溶液 ④用淀粉—KI试纸检验溶液中氧化性离子
⑤配制10%的硫酸钠溶液
A.①⑤ B.②⑤ C.①④ D.③④
(3)水洗时检验TiO2·x H2O已洗净的方法是
(4)下列可用于测定TiO2粒子大小的方法是 (填字母代号)
a.核磁共振氢谱 b.红外光谱法 c.质谱法 d.透射电子显微镜法
(5)滴定终点的现象是
(6)滴定分析时,称取TiO2(摩尔质量为Mg·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为 %
(7)下列操作会导致TiO2质量分数测定结果偏高的是
A. 滴定终点读取滴定管刻度时,俯视标准液液面
B. 配制标准溶液时,烧杯中的NH4Fe(SO4)2溶液有少量溅出
C. 容量瓶清洗之后,未干燥
D.配制标准溶液定容时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮限时训练四化学试卷(解析版) 题型:选择题
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol·L-1 的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A.开始加入合金的质量可能为16.4g
B.标准状况下产物NO的体积为22.4L
C.生成沉淀完全时消耗NaOH溶液的体积为100mL
D.参加反应的硝酸的物质的量为0.1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com