
| A£® | 5d | B£® | 6d | C£® | 7d | D£® | 8d |
·ÖĪö ĻąĶ¬Ģõ¼žĻĀ£¬ĘųĢåµÄĆܶČÖ®±ČµČÓŚĘäĦ¶ūÖŹĮæÖ®±Č£¬Éś³ÉµÄ»ģŗĻĘųĢå¶ŌĒāĘųµÄĻą¶ŌĆܶČĪŖd£¬Ōņ»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæĪŖ2dg/mol£¬øł¾ŻÖŹĮæŹŲŗćŌŁ½įŗĻM=$\frac{m}{n}$¼ĘĖćAµÄĦ¶ūÖŹĮ棬Ħ¶ūÖŹĮæŌŚŹżÖµÉĻµČÓŚĘäĻą¶Ō·Ö×ÓÖŹĮ森
½ā“š ½ā£ŗĻąĶ¬Ģõ¼žĻĀ£¬ĘųĢåµÄĆܶČÖ®±ČµČÓŚĘäĦ¶ūÖŹĮæÖ®±Č£¬Éś³ÉµÄ»ģŗĻĘųĢå¶ŌĒāĘųµÄĻą¶ŌĆܶČĪŖd£¬Ōņ»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæĪŖ2dg/mol£¬
¼ŁÉčÓŠ2molA·“Ó¦ŌņÉś³É3molB”¢2molC”¢2molD£¬Éś³ÉĪļµÄÖŹĮæ=2dg/mol”Į£Ø3+2+2£©mol=14dg£¬·“Ó¦Ē°ŗóÖŹĮæ²»±ä£¬ŌņAµÄÖŹĮæĪŖ14dg£¬ĘäĦ¶ūÖŹĮæ=$\frac{14dg}{2mol}$=7dg/mol£¬Ä¦¶ūÖŹĮæŌŚŹżÖµÉĻµČÓŚĘäĻą¶Ō·Ö×ÓÖŹĮ棬ĖłŅŌAµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ7d£¬
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ¶ØĀɼ°ĘäĶĘĀŪ£¬Ć÷Č·ĻąĶ¬Ģõ¼žĻĀ²»Ķ¬ĘųĢåĆܶČÓėĘäĻą¶Ō·Ö×ÓÖŹĮæµÄ¹ŲĻµŹĒ½ā±¾Ģā¹Ų¼ü£¬ŌŁ½įŗĻ»ł±¾¹«Ź½·ÖĪö½ā“š£¬ĢāÄæÄŃ¶Č²»“ó£®


 µŚ1¾ķµ„ŌŖŌĀæ¼ĘŚÖŠĘŚÄ©ĻµĮŠ“š°ø
µŚ1¾ķµ„ŌŖŌĀæ¼ĘŚÖŠĘŚÄ©ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molČĪŗĪĪļÖŹ¶¼ŗ¬ÓŠ6.02”Į1023øöŌ×Ó | |
| B£® | 0.012kg12C ŗ¬ÓŠ°¢·ü¼ÓµĀĀŽ³£ŹżøöĢ¼Ō×Ó | |
| C£® | ŌŚŹ¹ÓĆĦ¶ū±ķŹ¾ĪļÖŹµÄĮæµÄµ„Ī»Ź±£¬Ó¦ÖøĆ÷Į£×ÓµÄÖÖĄą | |
| D£® | ĪļÖŹµÄĮæŹĒ¹ś¼Źµ„Ī»ÖĘÖŠĘßøö»ł±¾ĪļĄķĮæÖ®Ņ» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | MgCl2 | B£® | ZnCl2 | C£® | BaCl2 | D£® | KCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ÆŗĻ·“Ó¦¾łĪŖŃõ»Æ»¹Ō·“Ó¦ | B£® | ½šŹōŃõ»ÆĪļ¾łĪŖ¼īŠŌŃõ»ÆĪļ | ||
| C£® | ÉÕ¼ī”¢“æ¼ī”¢ŹģŹÆ»Ņ¶¼ŹĒ¼ī | D£® | BaSO4”¢NaOH”¢HNO3¶¼ŹĒĒæµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
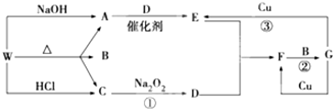
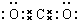 £¬FµÄŃÕÉ«ŗģ×ŲÉ«£®
£¬FµÄŃÕÉ«ŗģ×ŲÉ«£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
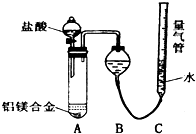 ĀĮĆ¾ŗĻ½šŅŃ³ÉĪŖĀÖ“¬ÖĘŌģ”¢»Æ¹¤Éś²śµČŠŠŅµµÄÖŲŅŖ²ÄĮĻ£®ŃŠ¾æŠŌѧĻ°Š”×éµÄČżĪ»Ķ¬Ń§£¬ĪŖ²ā¶Øijŗ¬Ć¾3%Ņ»5%µÄĀĮĆ¾ŗĻ½š£Ø²»ŗ¬ĘäĖüŌŖĖŲ£©ÖŠĆ¾µÄÖŹĮæ·ÖŹż£¬Éč¼ĘĻĀĮŠČżÖÖ²»Ķ¬ŹµŃé·½°ø½ųŠŠĢ½¾æ£®ĢīŠ“ĻĀĮŠæÕ°×£®
ĀĮĆ¾ŗĻ½šŅŃ³ÉĪŖĀÖ“¬ÖĘŌģ”¢»Æ¹¤Éś²śµČŠŠŅµµÄÖŲŅŖ²ÄĮĻ£®ŃŠ¾æŠŌѧĻ°Š”×éµÄČżĪ»Ķ¬Ń§£¬ĪŖ²ā¶Øijŗ¬Ć¾3%Ņ»5%µÄĀĮĆ¾ŗĻ½š£Ø²»ŗ¬ĘäĖüŌŖĖŲ£©ÖŠĆ¾µÄÖŹĮæ·ÖŹż£¬Éč¼ĘĻĀĮŠČżÖÖ²»Ķ¬ŹµŃé·½°ø½ųŠŠĢ½¾æ£®ĢīŠ“ĻĀĮŠæÕ°×£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äå»ÆµāÄÜÓė½šŹōŗĶ·Ē½šŹō·“Ó¦ | B£® | ĖüæÉÓėĖ®·“Ó¦£ŗIBr+H2O”śHBrO+HI | ||
| C£® | ĖüæÉKIČÜŅŗ·“Ó¦ KI+IBr”śKBr+I2 | D£® | ¹ĢĢåäå»ÆµāŹĒŅ»ÖÖ·Ö×Ó¾§Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
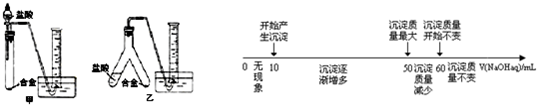
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com