
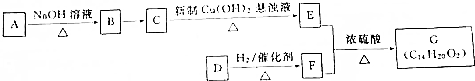
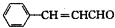 ��
�� ��
��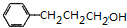 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$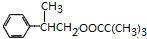 +H2O��CH3��3CCOOH+
+H2O��CH3��3CCOOH+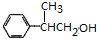 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$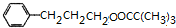 +H2O��
+H2O�� ��
������ ȡ����A��NaOH��Һ��Ӧ�����Һ���Թ��У����������ữ����������Һ����dz��ɫ����������˵��A�к�����ԭ�ӣ�A�ĺ˴Ź���������ʾΪ2��壬�ҷ������Ϊ9��2��˵��A�Ľṹ��һ�ֶԳƽṹ��A����Է�������Ϊ151������A�Ľṹ��ʽΪ��CH3��3CCH2Br��A�ڼ���������ˮ���BΪ��CH3��3CCH2OH��C����������ͭ����������Ӧ������B������CΪ��CH3��3CCHO��C������EΪ��CH3��3CCOOH��D���Է���������Ӧ��˵����ȩ����һ��������1molD����2molH2��Ӧ����1molF����D������̼����̼̼˫����D��F��G�ķ����о����б������ұ����ϵ�ȡ������ֻ��һ�������G�ķ���ʽ��֪��DΪ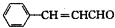 ��
�� ��1molD����2molH2��Ӧ����1molFΪ
��1molD����2molH2��Ӧ����1molFΪ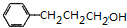 ��
��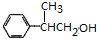 ��E��F����������Ӧ��GΪ
��E��F����������Ӧ��GΪ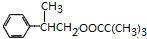 ��
��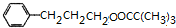 ���ݴ˴��⣮
���ݴ˴��⣮
��� �⣺ȡ����A��NaOH��Һ��Ӧ�����Һ���Թ��У����������ữ����������Һ����dz��ɫ����������˵��A�к�����ԭ�ӣ�A�ĺ˴Ź���������ʾΪ2��壬�ҷ������Ϊ9��2��˵��A�Ľṹ��һ�ֶԳƽṹ��A����Է�������Ϊ151������A�Ľṹ��ʽΪ��CH3��3CCH2Br��A�ڼ���������ˮ���BΪ��CH3��3CCH2OH��C����������ͭ����������Ӧ������B������CΪ��CH3��3CCHO��C������EΪ��CH3��3CCOOH��D���Է���������Ӧ��˵����ȩ����һ��������1molD����2molH2��Ӧ����1molF����D������̼����̼̼˫����D��F��G�ķ����о����б������ұ����ϵ�ȡ������ֻ��һ�������G�ķ���ʽ��֪��DΪ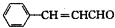 ��
�� ��1molD����2molH2��Ӧ����1molFΪ
��1molD����2molH2��Ӧ����1molFΪ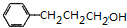 ��
��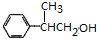 ��E��F����������Ӧ��GΪ
��E��F����������Ӧ��GΪ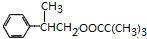 ��
��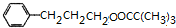 ��
��
��1����������ķ�����֪��A�Ľṹ��ʽΪ��CH3��3CCH2Br��A���еĹ���������ԭ�ӣ���B����C�ķ�Ӧ����Ϊ������Ӧ��D�Ľṹ��ʽΪ 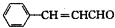 ��
�� ��
��
�ʴ�Ϊ����ԭ�ӣ�������Ӧ��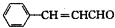 ��
�� ��
��
��2��CΪ��CH3��3CCHO��C������Cu��OH��2����Һ��Ӧ�Ļ�ѧ����ʽΪ����CH3��3CCHO+2Cu��OH��2+NaOH$\stackrel{��}{��}$��CH3��3CCOONa+Cu2O��+3H2O��
�ʴ�Ϊ����CH3��3CCHO+2Cu��OH��2+NaOH$\stackrel{��}{��}$��CH3��3CCOONa+Cu2O��+3H2O��
��3��DΪ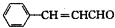 ��
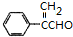
�� ��D�ж���ͬ���칹��������D����������ͬ�Һ��б�����ͬ���칹��Ϊ����������-CH=CH2��-CHO�����ڼ�����֣�
��D�ж���ͬ���칹��������D����������ͬ�Һ��б�����ͬ���칹��Ϊ����������-CH=CH2��-CHO�����ڼ�����֣�
�ʴ�Ϊ��3��
��4��EΪ��CH3��3CCOOH��E��F��Ӧ�Ļ�ѧ����ʽΪ ��CH3��3CCOOH+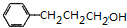 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$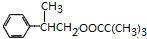 +H2O��CH3��3CCOOH+
+H2O��CH3��3CCOOH+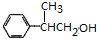 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$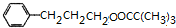 +H2O��
+H2O��
�ʴ�Ϊ����CH3��3CCOOH+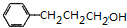 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$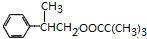 +H2O��CH3��3CCOOH+
+H2O��CH3��3CCOOH+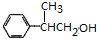 $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$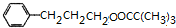 +H2O��
+H2O��
��5��FΪ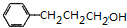 ��
��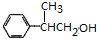 ��������������F��Ϊͬ���칹�壬����FeCl3��Һ����ɫ��˵���з��ǻ����۱�����������ȡ�������ұ����ϵ�һ����������֣�˵����ȡ����λ�ڱ����Ķ�λ�����������ĽṹΪ
��������������F��Ϊͬ���칹�壬����FeCl3��Һ����ɫ��˵���з��ǻ����۱�����������ȡ�������ұ����ϵ�һ����������֣�˵����ȡ����λ�ڱ����Ķ�λ�����������ĽṹΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ���Ҫ�Ը������Ϣ�������ã��ܽϺõĿ���ѧ���Ķ���ȡ��Ϣ������ȷ��A�Ľṹ��ʽ�ǹؼ����������Ʒ������Ʒ����Ͻ����ƶϣ�ע�����չ����ŵ�������ת�����Ѷ��еȣ�


 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����������� | ������ | |
| A | ��100mL�� 2mol•L-1H2SO4 | ����Ӧ������c��Na+��=c��SO42-�� |
| B | ��0.20molCaO | ��Һ��$\frac{c��O{H}^{-}��}{c��HC{O}_{3}^{-}��}$���� |
| C | ��200mL H2O | ����ˮ�������c��H+��•c��OH-������ |
| D | ��0.4molNaHSO4���� | ��Ӧ��ȫ����ҺpH��С��c��Na+�����䡡 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ħ�����ԼΪ22.4L•mol-1 | |
| B�� | �ڱ�״���£�1mol�κ�������ռ�������ԼΪ22.4L | |
| C�� | HNO3��Ħ��������63g | |
| D�� | ����������Ħ��������ȣ�����98g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��Br-��Cl-��SO42- | B�� | SCN-��Fe3+��Cl-��K+ | ||
| C�� | K+��Cu2+��SO42-��Na+ | D�� | Na+��ClO-��NO3-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2���������ԣ�������Ư��ֽ�� | |
| B�� | ������Һ��������ɫ�������ڼ���ⵥ�ʵĴ��� | |
| C�� | Fe�ڳ�������Ũ���ᷢ���ۻ���������������ʢ�����Ũ���� | |
| D�� | Zn���л�ԭ�Ժ͵����ԣ�������п�̸ɵ�صĸ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ĵ��뷽��ʽ����ЧӦ�ɱ�ʾΪ��HF��aq��?F-��aq��+H+��aq����H=+10.4 kJ•mol-1 | |
| B�� | NaFˮ��ʱ���Ȼ�ѧ����ʽΪF-��aq��+H2O��aq��=HF��aq��+OH-��aq����H=+67.7KJ•mol | |
| C�� | ��Һ�¶����ߺ�һ���ܴٽ�������ʵĵ��� | |
| D�� | ������0.1molHF��0.1molNaOH���������ʻ�Ϻ�ų�������Ϊ6.77KJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����һ�ַdz����õĽ��� | B�� | þ������������Ӧ��������þ | ||
| C�� | �Ƶ�Ӳ�ȴ� | D�� | ���ij�����������Al3O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
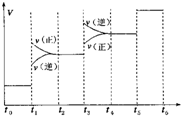 ������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϣ�
������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com