
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2LiNH2+LiH,下列有关说法正确的是( )
A.Li2NH中N的化合价是-1
B.该反应中H2既是氧化剂又是还原剂
C.Li+和H-的离子半径相等
D.此法储氢和钢瓶储氢的原理相同
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
下列各组原子中,彼此化学性质一定相似的是( )
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y 原子
原子
D.最 外层都只有一个电子的X、Y原子
外层都只有一个电子的X、Y原子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知具有碳碳双键结构的有机物可被碱性高锰酸钾溶液氧化成二元醇,如H2C===CH2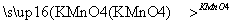 HOCH2CH2OH。现以CH2===C(CH3)2为原料按下列方式合成环状化合物D和高分子化合物G。
HOCH2CH2OH。现以CH2===C(CH3)2为原料按下列方式合成环状化合物D和高分子化合物G。
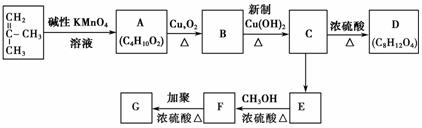
(1)A→B的反应类型是________,C→E的反应类型是________,E→F的反应类型是________。
(2)D的结构简式是________,G的结构简式是________。
(3)B→C的化学方程式是________________________________________________________________________。
(4)E→F的化学方程式是________________________________________________________________________。
(5)C物质的同分异构体中,与C所含官能团种类和数目都相同的同分异构体有________种(不包括C)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是( )
①维生素C具有还原性,在人体内起抗氧化作用(2009·天津理综,1A)
②NO2溶于水时发生氧化还原反应(2012·天津理综,2C)
③1 mol Cl2参加反应转移电子数一定为2NA(2010·福建理综,7C)
④阴离子都只有还原性(2008·北京理综,8B)
⑤BaSO3和H2O2的反应为氧化还原反应
A.①②⑤ B.②③⑤ C.③④⑤ D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,颜色的变化与氧化还原反应有关的是( )
A.往紫色石蕊溶液中加入盐酸,溶液变红
B.饱和FeCl3溶液在沸水中变成红褐色胶体
C.向FeSO4溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色
D.SO2使滴有酚酞的NaOH溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
关于反应Zn+2HNO3+NH4NO3===N2↑+3H2O+Zn(NO3)2,下列判断正确的是( )
A.生成1 mol N2,电子转移总数为3NA
B.生成1 mol N2,电子转移总数为5NA
C.溶解1 mol Zn,电子转移总数为2NA
D.溶解1 mol Zn,电子转移总数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为________。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为________(填化学式)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定的溶液中,能大量共存的划“√”,不能大量共存的划“×”
(1)含有大量Fe3+的溶液:Na+、SCN-、Cl-、I-( )
(2)含有大量NO 的溶液:H+、Fe2+、Cl-、SO
的溶液:H+、Fe2+、Cl-、SO ( )
( )
(3)常温下,pH=12的溶液:K+、Cl-、SO ( )
( )
(4)c(H+)=0.1 mol·L-1的溶液:Na+、NH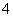 、SO
、SO 、S2O
、S2O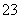 ( )
( )
(5)使pH试纸显蓝色的溶液:Cu2+、NO 、Fe3+、SO
、Fe3+、SO ( )
( )
(6)与铝粉反应放出H2的无色溶液:NO 、Al3+、Na+、SO
、Al3+、Na+、SO ( )
( )
(7)使红色石蕊试纸变蓝的溶液:SO 、CO
、CO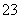 、Na+、K+( )
、Na+、K+( )
(8)常温下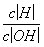 =1×10-12的溶液:K+、AlO
=1×10-12的溶液:K+、AlO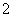 、CO
、CO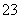 、Na+( )
、Na+( )
(9)中性溶液:Fe3+、Al3+、NO 、SO
、SO ( )
( )
(10)使甲基橙变红色的溶液:Mg2+、K+、SO 、SO
、SO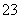 ( )
( )
(11)c(H+)水=10-12 mol·L-1的溶液:Na+、K+、CO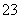 、SO
、SO ( )
( )
(12)使酚酞变红色的溶液:Na+、Cu2+、Fe2+、NO ( )
( )
(13)0.1 mol·L-1的Na2CO3溶液:Al3+、SO 、Cl-、K+( )
、Cl-、K+( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com