
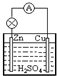
| A.Cu为负极,Zn为正极 |
| B.负极反应为:Zn-2e-=Zn2+ |
| C.正极反应为:Cu2++2e-=Cu |
| D.正极发生氧化反应,负极发生还原反应 |
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 目的 | 粗铜的精炼 | 验证NaCl溶液(含酚酞)的产物 | 在铁制品上镀铜 | 构成原电池 |
| 装置 | 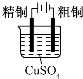 | 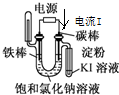 |  | 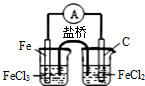 |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
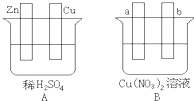
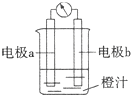
| A.原电池是将化学能转化成电能的装置 |
| B.原电池的负极发生氧化反应 |
| C.图中a极为镁条、b极为锌片时,导线中会产生电流 |
| D.图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
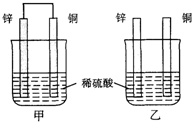
| A.甲中铜片是负极 |
| B.两烧杯中铜片表面均无气泡产生 |
| C.产生气泡的速度甲比乙快 |
| D.两烧杯中溶液的pH均减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CaO+H2O═Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3═Cu(NO3)2+2Ag,装置中的盐桥中可以是由KCl饱和溶液制得的琼脂 |
| C.因为铁的活动性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可被设计成原电池 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
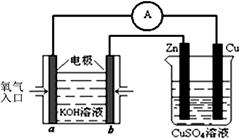
| A.甲、丙中是化学能转变为电能,乙中是电能转变为化学能 |
| B.C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 |
| C.C1和C3放出的气体相同,铜片和铁片放出的气体也相同 |
| D.甲、乙中溶液的pH值逐渐升高,丙中溶液的pH逐渐减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g) ΔH1
CH3OH(g) ΔH1 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com