
【题目】某种氨硼烷(NH3·BH3)电池装置如图所示(未加入氨硼烷之前,两极室内液体质量相等),电池反应为NH3·BH3+3H2O=NH4BO2+4H2O(不考虑其他反应的影响)。下列说法错误的是( )
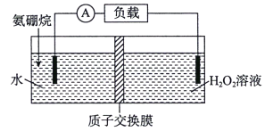
A.氨硼烷中N和B的杂化方式不同
B.电池正极的电极反应式为H2O2+2H++2e-=2H2O
C.其他条件不变,向H2O2溶液中加入适量硫酸能增大电流强度
D.若加入的氨硼烷全部放电后左右两极室内液体质量差为3.8g,则电路中转移1.2mol电子
【答案】A
【解析】
根据电池反应为NH3·BH3+3H2O=NH4BO2+4H2O可知,左侧NH3BH3为负极,失电子发生氧化反应,电极反应式为:NH3BH3+2H2O-6e-=NH4BO2+6H+,右侧H2O2为正极,得到电子发生还原反应,电极反应式为3H2O2+6H++6e-=6H2O。
A. 氨硼烷中N是sp3杂化,B是sp2杂化,其杂化方式不同,A错误;
B. 右侧H2O2为正极,得到电子发生还原反应,电极反应式为H2O2+2H++2e-=2H2O,B正确;
C. 正极上消耗氢离子,其他条件不变,向H2O2溶液中加入适量硫酸能增大电流强度,C正确;
D. 未加入氨硼烷之前,两极室内液体质量相等,通入后,负极电极反应式为:NH3BH3+2H2O-6e-=NH4BO2+6H+,正极电极反应式为:3H2O2+6H++6e-=6H2O,假定转移6mol电子,则左室质量增加=31g-6g=25g,右室质量增加6g,两极室质量相差19g,理论上转移6mol电子,工作一段时间后,若左右两极室质量差为3.8g,则电路中转移1.2mol电子,D正确;故答案为:A。


科目:高中化学 来源: 题型:
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
A.电池的电解质溶液为碱性溶液,阳离子向正极移动
B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.5mol/L NaOH溶液和0.5mol/L硫酸溶液进行中和热的测定。
Ⅰ.准备仪器
(1)环形玻璃搅拌棒__________(填“能”或“不能”)改为环形金属(如铜)棒,其原因是__________。
(2)碎泡沫的作用是______________,终止温度应为反应的最________(填“高”或“终”)温度。
II.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
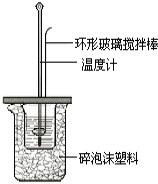
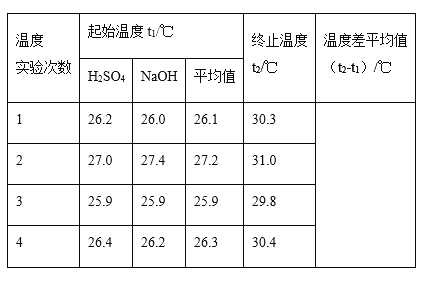
(1)四次实验所得到的温度平均值为__________℃。
(2)取50mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如表。
①近似认为0.5mol/LNaOH溶液和0.5mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J·g-1·℃-1。则中和热△H =_____(取小数点后一位)。
②上述实验数值结果与573KJ·mol-1有偏差,产生偏差的原因可能是(填字母)_____。
a.实验装置保温、隔热效果差
b. 量取NaOH溶液的体积时仰视读数
c. 分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.反应时未用搅拌器搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可利用反应2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH检测乙醇。下列说法错误的是( )
A.基态Cr3+的核外电子排布式为3d3
B.[Cr(H2O)6]3+中与Cr3+形成配位键的原子是氧原子
C.CH3COOH分子中含有7个![]() 键
键
D.已知CrO42-是以Cr为中心的四面体结构,则Cr2O72-结构中含有两个四面体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组拟用酸性KMnO4溶液与H2C2O4溶液的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L酸性KMnO4溶液)/mL | m(MnSO4)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.5 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |