
【题目】同分异构体指的是相同分子式不同分子结构的化合物,它描述的对象主体是化合物。同素异形体、同位素、同系物描述的对象主体依次为
A.单质、原子、化合物B.元素、单质、化合物
C.无机化合物、元素、有机化合物D.原子核、原子、分子
科目:高中化学 来源: 题型:
【题目】在t℃时,将agNH3完全溶于水,得到VmL溶液,设该溶液的密度为ρg·cm-3,质量分数为ω,其中含NH4+的物质的量为bmol。下列叙述中不正确的是
A.溶质的质量分数ω=![]() ×100%
×100%
B.溶质的物质的量浓度c=1000a/17Vmol·L-1
C.溶液中c(OH-)=1000b/Vmol·L-1+c(H+)
D.上述溶液中再加入VmL水后,所得溶液中溶质的质量分数小于0.5ω
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列有关说法不正确的是
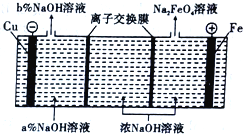
A. 右侧电极反应方程式:Fe+8OH--6e-=FeO42-+4H2O
B. 左侧为阳离子交换膜,当Cu电极生成1mol气体时,有2molNa+通过阳离子交换膜
C. 可以将左侧流出的氢氧化钠补充到该装置中部,以保证装置连续工作
D. Na2FeO4具有强氧化性且产物为Fe3+,因此可以利用Na2FeO4除去水中的细菌、固体颗粒以及Ca2+等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO42H2O)是无公害型冷却水系统的金属缓蚀剂,由钼精矿(主要成分是MoS2,含少量PbS等)制备钼酸钠晶体的部分流程如图所示

(1)Na2MoO42H2O中钼元素的化合价为____________。
(2)焙烧时为了使钼精矿充分反应,可采取的措施是____________(答出一条即可)。
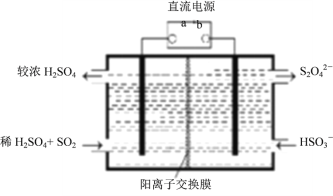
(3)焙烧过程中钼精矿发生的主要反应的化学方程式为MoS2+O2![]() MoO3+SO2(未配 平),该反应中氧化产物是____________(填化学式);当生成1molSO2时,该反应转移的电子的物质的量为_________mol。利用下图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2。阳极的电极反应式为__________________________,在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO42-生成,该反应的离子方程式为____________________________________________________。
MoO3+SO2(未配 平),该反应中氧化产物是____________(填化学式);当生成1molSO2时,该反应转移的电子的物质的量为_________mol。利用下图所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2。阳极的电极反应式为__________________________,在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO42-生成,该反应的离子方程式为____________________________________________________。
(4)碱浸时,MoO3与Na2CO3溶液反应的离子方程式为__________________________。
(5)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因____________________________________。
(6)过滤后的碱浸液结晶前需加入Ba(OH)2固体以除去SO42-,当BaMoO4开始沉淀时, SO42-去除率为97.5%,已知碱浸液中c(MoO42-)=0.40molL-1,c(SO42-)=0.040molL-1,Ksp(BaSO4)=1.0×10-10、则Ksp(BaMoO4)=________________[加入Ba(OH)2固体引起的溶液体积变化可忽略]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表是某位生物教师的肝肾糖脂血液化验单部分内容:
已知:1摩尔(mol)等于1000毫摩尔(mmol),血液中葡萄糖简称血糖,分子式为C6H12O6,请根据以上信息回答下列问题:
项目名称 | 数据 | 参考值 |
尿素氮 | 2.95 | 2.00﹣6.10mmol.L﹣1 |
葡萄糖 | 4.50 | 3.89﹣6.11mmol.L﹣1 |
总胆固醇 | 3.75 | <5.20mmol.L﹣1 |
甘油三酯 | 1.80↑ | <1.70mmol.L﹣1 |
(1)这位教师的血糖含量属___(填“正常”、“偏高”或“偏低”)。
(2)这位教师的1mL血液中含葡萄糖___g。
Ⅱ.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。表是500mL“鲜花保鲜剂”中含有的成分,阅读并回答下列问题:
成分 | 成分的质量(g) | 摩尔质量(gmol﹣1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.02 | 170 |
(1)下列“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为___。
(2)配制上述“鲜花保鲜剂”所的仪器有烧杯、玻璃棒、药匙、托盘天平(带砝码)、___(填所缺仪器的名称)。
(3)若要配制0.5mol/L500mL的硫酸溶液,现有质量分数为98%、密度为1.84g·cm﹣3的浓硫酸。实验室有15mL、20mL、50mL量筒,应选用___mL量筒最好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质结构与性质)
2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB族元素对应离子的萃取,如La3+、Sc2+。写出基态二价钪离子(Sc2+)的核外电子排布式:________,其中电子占据的轨道数为________个。
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为________,羟基间的相互作用力为________。
(3)不同大小的苯芳烃能识别某些离子,如:![]() 、SCN-等。一定条件下,SCN-与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式______________________________。
、SCN-等。一定条件下,SCN-与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式______________________________。
(4)NH3分子在独立存在时H-N-H键角为106.7°。如图 [Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因:______。
(5)橙红色的八羰基二钴[Co2(CO)8]的熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂。该晶体属于________晶体,八羰基二钴在液氨中被金属钠还原成四羰基钴酸钠[NaCo(CO)4],四羧基钴酸钠中含有的化学键为_________________。
(6)已知C60分子结构和C60晶胞示意图(如图Ⅱ、图Ⅲ所示):

则一个C60分子中含有σ键的个数为________,C60晶体密度的计算式为________ g·cm-3。(NA为阿伏伽德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目。____________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4—+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4—+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:______,MnO![]() +Fe2++H+=Mn2++Fe3++H2O
+Fe2++H+=Mn2++Fe3++H2O
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 16 克 CO 和 CO2 的混合气体通过足量的灼热的氧化铜后,得到气体的总质量为 22 克,求原混合气 体中 CO 的质量分数?_____若将所得的气体再通入到 100 克质量分数为 22.2%的澄清石灰水中,求所得沉淀的质量为多少克?________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com