
试样X由FeO和CuO组成。取质量相等的两份试样按如下所示流程图进行实验:
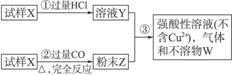
(1)请写出步骤③中所发生的全部反应的离子方程式。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,每份试样X中氧化铜的质量为__________(用m表示)。
(1)Fe+Cu2+====Fe2++Cu Fe+2H+====Fe2++H2↑ (2)0.625m
按图顺序正推,依次写出①-③的各步反应:
①FeO+2HCl====FeCl2+H2O CuO+2HCl====CuCl2+H2O
②FeO+CO![]() Fe+CO2 CuO+CO
Fe+CO2 CuO+CO![]() Cu+CO2
Cu+CO2
③Fe+Cu2+====Fe2++Cu Fe+2H+====Fe2++H2↑
(2)溶液Y是HCl、FeCl2、CuCl2的混合液,Z是Fe、Cu的混合物。Y与Z相混,经③所得溶液呈现强酸性且不含Cu2+,表明Y中的CuCl2已全部被Fe还原,而且HCl过量,则表明Fe无剩余,不溶物W全部为Cu。此Cu是两份X试样中所含CuO转变而来,故每份中m(CuO)=0.5m×(80/64)=0.625m。


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com